Texto Completo acta: 157C5A
N°
42769-MAG-S-MINAE
(Este
decreto ejecutivo fue derogado por el artículo 3° aparte 1) del decreto
ejecutivo N° 43838 del 14 de diciembre del 2023 "Reglamento Técnico RTCR
509:2022. Insumos Agrícolas. Plaguicidas Sintéticos Formulados, Ingrediente
Activo Grado Técnico, Coadyuvantes, Vehículos Físicos y Sustancias Afines de
Uso Agrícola. Registro")
EL PRESIDENTE DE LA REPÚBLICA
EL MINISTRO DE AGRICULTURA Y GANADERÍA, EL MINISTRO DE SALUD Y
LA MINISTRA DE AMBIENTE Y ENERGÍA
Con fundamento en las atribuciones y facultades conferidas en los
artículos, 46, 47, 50 y 140, incisos 3) y 18) y 146 de la Constitución
Política; artículos 27.1 y 28.2.b) de la Ley General de la Administración
Pública, Nº 6227 del 2 de mayo de 1978; artículo 2 inciso e), artículo 5,
incisos c), d) y o), del 23 al 39, concordantes de la Ley de Protección
Fitosanitaria, Nº 7664 del 8 de abril de 1997; artículos 1, 2, 4, 7, 244, 245,
252 de la Ley General de Salud, Nº 5395 del 30 de octubre de 1973; artículos 2
inciso b), c) y g) de la Ley Orgánica del Ministerio de Salud, concordantes, Nº
5412 del 8 de noviembre de 1973; artículo 50, de la Ley de Biodiversidad, Nº
7788 de 30 de abril de 1998; Ley de Uso, Manejo y Conservación de Suelos, Nº
7779 de 30 de abril de 1998; Ley Orgánica del Ministerio de Ambiente, Energía,
Nº 7152 de 5 de junio de 1990; artículos 1, 2, 4, 60, de la Ley Orgánica del
Ambiente, Nº 7554 del 4 de octubre de 1995; Ley del Sistema Nacional para la
Calidad, Nº 8279 del 2 de mayo de 2002; Ley de Promoción de la Competencia y
Defensa Efectiva del Consumidor, Nº 7472 del 20 de diciembre de 1994; Ley de
Protección al Ciudadano del Exceso de Requisitos y Trámites Administrativos, Nº
8220 del 4 de marzo de 2002; Ley de Marcas y Otros Signos Distintivos, Nº 7978
del 6 de enero de 2000; Ley de Información no Divulgada Nº 7975 del 4 de enero
de 2000; Ley Nº 7475 del 20 de diciembre de 1994, Aprobación del Acta Final en
que se Incorporan los Resultados de la Ronda Uruguay de Negociaciones
Comerciales Multilaterales.
CONSIDERANDO:
I. Que el artículo 50 de la Constitución Política consagra el derecho de
todas las personas a un ambiente sano y ecológicamente equilibrado, siendo el
deber del Estado garantizar, defender y preservar ese derecho.
II. Que el artículo 46 de la Constitución Política establece el derecho
constitucional de los consumidores y usuarios a la protección de su salud,
ambiente, seguridad e intereses económicos, así como a recibir información
adecuada y veraz, a la libertad de elección y a un trato equitativo.
III. Que uno de los objetivos de la Ley de Protección Fitosanitaria es
regular el uso y manejo de sustancias químicas para aplicarlas en la
agricultura, incluyendo su registro e importación, a la vez que se procura la
protección de la salud humana y el ambiente. Por ello las normas jurídicas y
técnicas relativas a la protección fitosanitaria deben ser interpretadas de
conformidad con el deber constitucional del Estado de actuar en prevención del
riesgo ambiental y de la protección de la salud humana y animal.
IV. Que las sustancias químicas para el uso en el combate y control de
plagas, representan un componente importante en los costos de producción e
influyen en la rentabilidad y competitividad de los productos agrícolas
convencionales en los mercados nacionales e internacionales. Asimismo,
presentan costos para el Estado y la sociedad asociados a externalidades
negativas producidas por su uso.
V. Que las sustancias químicas para uso agrícola representan un riesgo
potencial para la salud humana y animal, el ambiente y la sanidad vegetal, por
lo que su control requiere la participación integrada y coordinada del
Ministerio de Agricultura y Ganadería, el Ministerio de Salud y el Ministerio
de Ambiente y Energía, de conformidad con sus competencias.
VI. Que el legislador le confirió al Servicio Fitosanitario del Estado,
órgano desconcentrado del Ministerio de Agricultura y Ganadería, la competencia
de administrar el registro de sustancias químicas para uso agrícola, incluyendo
el registro de Ingrediente Activo Grado Técnico (en adelante IAGT).
VII. Que el marco jurídico nacional confiere competencias y legitimidad
a los Ministerios de Ambiente y Energía y de Salud, para participar en el
Registro de IAGT.
VIII. Que es fundamental que el sistema de registro de IAGT opere con
fluidez a efecto de que los productores agrícolas tengan acceso a nuevas
alternativas en el control de plagas, a la vez que se desincentive el uso de
plaguicidas obsoletos o prohibidos a nivel mundial o altamente peligrosos a la
luz del desarrollo científico y tecnológico.
IX. Que la Organización para la Cooperación y el Desarrollo Económicos
(en adelante OCDE) cuenta con sesenta años de experiencia y conocimiento en el
diseño y promoción de las políticas públicas con el fin último de procurar una
vida mejor para las personas, siendo la gestión ambiental una de sus áreas de
trabajo.
X. Que, en materia de agricultura, la OCDE reconoce la complejidad a la
que se enfrenta el sector agrícola el cual debe proveer alimentos de calidad a
una población mundial creciente, a la vez que se le exige la reducción del
impacto ambiental y la preservación de los recursos naturales para las futuras
generaciones.
XI. Que en relación con los plaguicidas de uso agrícola el objetivo de
la OCDE es colaborar con los gobiernos en el establecimiento de esquemas de
cooperación y en la evaluación de los riesgos asociados a estos productos, de
manera que el proceso de aprobación o registro de IAGT más seguros se realice
de manera más expedita y eficiente. Cada gobierno mantiene su soberanía en la
toma final de decisiones.
XII. Que la OCDE elaboró guías para la presentación de la información
con el objetivo de facilitar la evaluación de los IAGT minimizando la
duplicación del esfuerzo tanto para la industria como para los gobiernos; éstas
guías se basan en la constatación de que los datos requeridos para el registro
de agroquímicos se encuentran ampliamente armonizados entre los países miembros
de la organización.
XIII. Que las regulaciones correspondientes al registro de IAGT se
consideran procedimientos de evaluación de la conformidad en los términos del
Acuerdo sobre Obstáculos Técnicos al Comercio (AOTC) de la Organización Mundial
del Comercio (OMC).
XIV. Que el reconocimiento de los procedimientos de evaluación de la
conformidad entre los países miembros de la OMC se establece en el artículo 6
del AOTC según el cual "los Miembros se asegurarán de que, cada vez que
sea posible, se acepten los resultados de los procedimientos de evaluación de
la conformidad de los demás Miembros, aun cuando esos procedimientos difieran
de los suyos, siempre que tengan el convencimiento de que se trata de
procedimientos que ofrecen un grado de conformidad con los reglamentos técnicos
o normas pertinentes equivalente al de sus propios procedimientos".
XV. Que el Servicio Fitosanitario del Estado, el Ministerio de Salud y
el Ministerio de Ambiente y Energía analizaron el documento de la OCDE
denominado Guía para los Reportes de Evaluación de Datos de Productos de
Protección de las Plantas y sus Sustancias Activas -Revisión 3, de abril de
2008 (OECD Guidance for Country Data Review Reports on Plant Protection
Products and their Active Substances - Revision 3, April 2008 por su título
original) para el registro o aprobación de IAGT, concluyendo que la información
requerida y analizada a partir de esa guía en las diferentes áreas de sus
competencias, brinda un nivel de protección similar o superior al requerido por
la normativa nacional para el registro de IAGT y permiten alcanzar los mismos
objetivos que se contemplan en la legislación costarricense. Asimismo, se
reconoce que el AOTC brinda el marco jurídico requerido para analizar la
petición de reconocimiento de evaluaciones para el registro de IAGT que
cualquier Miembro de la OMC solicite.
XVI. Que la presente propuesta normativa se ajusta al supuesto de
excepción previsto en el artículo 2 inciso e) de la Directriz N° 052-MP-MEIC,
denominada "Moratoria a la creación de nuevos trámites, requisitos o procedimientos
al ciudadano para la obtención de permisos, licencias o autorizaciones",
en el tanto es una iniciativa promovida dentro del marco de ejecución del
proyecto de la Ventanilla Única de Inversión que tiene por objeto la mejora de
procesos, la simplificación de trámites, la reducción de tiempos y plazos de
resolución en beneficio del ciudadano; en virtud de lo anterior, se concluye
que el beneficio de dicha regulación es mayor al de su inexistencia.
XVII. Que de conformidad con lo establecido en el artículo 12 bis del
Decreto Ejecutivo No. 37045 del 22 de febrero de 2012 y su reforma "Reglamento
a la Ley de Protección al Ciudadano del Exceso de Requisitos y Trámites
Administrativos", esta regulación cumple con los principios de mejora
regulatoria, de acuerdo con el informe No. DMR-AR-INF-053-20 de 15 de setiembre
del 2020, emitido por la Dirección de Mejora Regulatoria y Reglamentación
Técnica del Ministerio de Economía, Industria y Comercio.
POR TANTO;
DECRETAN:
Reglamento para optar por el Registro de Ingrediente Activo Grado
Técnico mediante el
reconocimiento de la evaluación de los estudios técnicos aprobados por
las Autoridades
Reguladoras de los países miembros de la Organización para la
Cooperación y el
Desarrollo Económicos (OCDE) o las Autoridades Reguladoras de los países
adherentes
al Sistema de Aceptación Mutua de Datos de la OCDE.
Capítulo I
Disposiciones generales
Artículo 1. Objeto. Regular el registro de Ingredientes Activos Grado
Técnico (IAGT) con data completa que han sido aprobados previamente por las
Autoridades Reguladoras de i) los países miembros de la OCDE o, ii) de los
países que son adherentes plenos al sistema de aceptación mutua de datos (AMD)
de esa organización, mediante el reconocimiento de la evaluación de los
estudios técnicos aprobados que se señalan en el punto I.A del Anexo III del
presente reglamento.
Ficha articulo
Artículo 2. Ámbito de aplicación. El presente reglamento aplica al IAGT que se
pretenda registrar, siempre que haya sido registrado o autorizado previamente
por la Autoridad Reguladora de un país miembro de la OCDE o de un país
adherente pleno al sistema de AMD de esa organización, de conformidad con las disposiciones
que se establecen en este reglamento. El IAGT podrá estar registrado o
autorizado en los países antes indicados solo o formando parte de un producto
sintético formulado o vehículo físico.
Ficha articulo
Artículo 3. Definiciones. Los términos y definiciones aplicados en este
reglamento son los que se indican a continuación:
Aditivos: componentes añadidos al ingrediente activo antes de fabricar el
producto formulado con objeto de mantener su estabilidad y facilitar su
manipulación.
Autoridad Competente (AC): es el Servicio Fitosanitario del Estado
(SFE), como ente competente para la administración de los registros de IAGT de
uso agrícola.
Autoridades revisoras competentes: son el Ministerio de Salud (MINSA), el
Ministerio de Ambiente y Energía (MINAE), y las dependencias competentes del
SFE del Ministerio de Agricultura y Ganadería (MAG).
Autoridad reguladora: es la agencia, institución o dependencia de un país
miembro de la OCDE o de un país adherente pleno al sistema de AMD de esa
organización, competente para la evaluación, aprobación y/o registro del IAGT
que se solicita para registro en Costa Rica.
Clase de plaguicida: Hace referencia al tipo de actividad u organismo
objetivo para el cual se utiliza el plaguicida
Data completa: para efectos de interpretación de este reglamento,
corresponde a la totalidad de requisitos que se solicitan para el registro de
un IAGT de acuerdo con el Anexo III de este reglamento.
Datos de prueba: los datos de prueba son información no divulgada
que incluye la información, datos o documentos sobre la seguridad y eficacia de
un IAGT cuya elaboración suponga un esfuerzo considerable, que no hayan sido
divulgados al público y que sean exigidos por la Autoridad Reguladora con el
fin de otorgar el registro en el país de dicho IAGT. Esta información se aporta
dentro del legajo de información técnica e incluye los datos o documentos sobre
los estudios toxicológicos, los estudios eco-toxicológicos, los estudios sobre
los efectos en el medio abiótico, y las propiedades fisicoquímicas y los
métodos analíticos sobre la seguridad, eficacia, calidad y de residuos del
IAGT.
Declaración jurada notarial: es aquella declaración rendida bajo fe de juramento
ante Notario Público y debidamente protocolizada.
Entidad química: es el ingrediente activo responsable de la acción
biocida o fisiológica.
Estudios técnicos: son los estudios sobre las propiedades
fisicoquímicas, los efectos tóxicos en especies mamíferas, estudios
ecotoxicológicos, destino y comportamiento ambiental, estudios sobre la ruta de
degradación del IAGT, información con respecto a la seguridad (ambiental y
laboral) y los métodos analíticos y su respectiva validación para la determinación
de IAGT, impurezas relevantes, residuos en cultivos, suelo, agua y aire.
Etiqueta: material escrito, impreso o gráfico que va en la superficie del envase
adherido (pegado) o estampado al recipiente del producto, que identifica y
describe el producto contenido en el envase.
Evaluación técnica ante las Autoridades revisoras competentes: proceso donde se
realiza la revisión de la información administrativa, técnica y confidencial.
Fabricante: una compañía u otra entidad pública o privada o cualquier persona física
o jurídica dedicada (directamente o por medio de un agente o de una entidad por
ella controlada o contratada) al negocio o a la función de fabricar un
ingrediente activo plaguicida, o de preparar su formulación o producto.
Grupo o familia química de plaguicida: Se entiende por
grupo o familia química de plaguicida el grupo basado en la estructura química
o grupos de productos químicos que comparten características y modo de acción
comunes, utilizando como referencia lo establecido en los organismos internaciones
reconocidos.
Guía de Admisibilidad: es el documento para la verificación inicial de
cumplimiento de los requisitos para el registro de IAGT por reconocimiento de
la evaluación de los estudios técnicos.
Impurezas: es un subproducto que surge de la fabricación del ingrediente activo o
se deriva
del ingrediente
activo durante la formulación o almacenamiento.
Impurezas relevantes: un subproducto de la fabricación o almacenamiento
de un plaguicida que, en comparación con el ingrediente activo, es toxicológicamente
significativo para la salud o el medio ambiente, es fitotóxico a las plantas
tratadas, provoca mancha en cultivos de alimentos, afecta a la estabilidad del
plaguicida, o causa cualquier otro efecto adverso. Una impureza puede ser no
relevante en un plaguicida o producto y relevante en otro, a pesar de que se
produce en ambos, porque la relevancia se determina por los peligros de
impurezas relativos a la del ingrediente activo. En general, las impurezas
relevantes son aquellas definidas como tal y hechas públicas por organismos
tanto internacionales como intergubernamentales de referencia como la FAO,
EFSA, APVMA, EPA y BVL.
Impurezas no relevantes: son las impurezas que, comparadas con el
ingrediente activo, no son toxicológicamente significativas para la salud o el
ambiente. En general las impurezas no relevantes tienen límites de
especificación de fabricación igual o mayor a un gramo por kilogramo (g/kg).
Ingrediente activo: para efectos de este reglamento se entenderá como
entidad química.
Ingrediente activo grado técnico (IAGT): el ingrediente
activo grado técnico se puede encontrar bajo dos denominaciones TC (material
técnico), y TK (concentrado técnico). El TC tiene normalmente una concentración
elevada de ingrediente activo; puede tener aditivos esenciales tales como
estabilizantes, pero no contiene diluyentes o solventes. El TK por su lado,
contiene normalmente una concentración menor, ya sea porque se ha agregado un
disolvente a un TC o porque puede ser impráctico o indeseable aislar el
ingrediente activo del disolvente, impurezas, entre otros. Además, el TK puede
tener aditivos esenciales tales como estabilizantes, así como diluyentes y
solventes.
Información administrativa: es toda información calificada y clasificada
como tal por este reglamento. Tendrán acceso a esta información los
funcionarios de las diferentes Autoridades revisoras competentes involucradas
en la evaluación, terceros a los que la ley les confiera ese derecho y los
autorizados por el registrante.
Información confidencial: es toda información calificada y clasificada como
tal por este reglamento y la normativa vigente en materia de información no
divulgada. Tendrán acceso a esta información únicamente los funcionarios que el
SFE mantiene en el registro de firmas.
Además, las Autoridades revisoras competentes deberán autorizar por
escrito, ante el SFE, los funcionarios que tendrán acceso a la información
confidencial. Las autoridades con acceso a la información confidencial no
requerirán autorización previa del titular de cualquier registro para la
revisión del expediente.
Información técnica: es toda información calificada y clasificada como
tal por este reglamento. Tendrán acceso a esta información los funcionarios de
las diferentes Autoridades revisoras competentes involucradas en la evaluación,
terceros a los que la ley les confiera ese derecho y los autorizados por el
registrante.
Material de referencia certificado de IAGT y sustancias relacionadas: material de
referencia del IAGT y sustancias relacionadas, acompañado de un certificado,
donde uno o varios valores de sus propiedades especificadas están certificadas
por un procedimiento que establece su trazabilidad a una realización precisa de
la unidad en la cual los valores de las propiedades específicas se encuentran
expresados y para el cual cada valor certificado se encuentra acompañado de una
incertidumbre con la indicación de un nivel de confianza.
Nombre comercial: es el nombre con el que el registrante identifica
un producto determinado para su comercialización.
Nombre genérico o común: es el nombre común del IAGT aprobado por algún
organismo oficial de estandarización internacional.
Nombre químico: se refiere al nombre de la(s) molécula(s) del
ingrediente activo de un producto aprobado por algún organismo oficial de
estandarización internacional, por ejemplo, IUPAC.
Países adherentes al Sistema de Aceptación Mutua de Datos (AMD) de la
OCDE: son los países no miembros de la OCDE donde se realizan estudios
utilizando métodos de prueba estándares de la OCDE y que han sido evaluados y
aprobados en cuanto a Buenas Prácticas de Laboratorio y son adherentes plenos
al sistema de AMD de esa organización. Son adherentes plenos del sistema de AMD
los siguientes países: India, Argentina, Brasil, Malasia, Suráfrica y Singapur,
así como los países que a futuro sean aprobados por la OCDE en dicha condición.
Plaguicida sintético formulado: es el producto comercial destinado al uso
agrícola para el combate de plagas que ha sido preparado a partir de uno o
varios IAGT u otro proceso de producción.
Producto agroquímico nuevo: es aquel IAGT que no contiene una entidad
química que se encuentre en un registro que se haya otorgado previamente en
Costa Rica, como IAGT o formando parte de un plaguicida sintético formulado o
vehículo físico.
Reconocimiento de la evaluación aprobada de los
estudios técnicos: es el proceso mediante el cual
las Autoridades revisoras competentes verifican el contenido, los resultados y
referencias bibliográficas de los estudios técnicos indicados en el Reporte de
Evaluación realizado por la Autoridad reguladora del país miembro de la OCDE o
de un país adherente pleno al sistema de AMD de esa organización.
Para el
reconocimiento de la evaluación de los estudios técnicos, el IAGT registrado o
autorizado previamente por la Autoridad reguladora debe ser de la misma empresa
o titular de la información, y misma concentración mínima, respecto al que se
solicita registrar en Costa Rica.
Esta
verificación no implica una nueva evaluación de cada estudio técnico por parte
de las Autoridades revisoras competentes.
(Así
reformada la definición anterior por el artículo 1° del decreto ejecutivo N°
43563 del 28 de mayo de 2022)
Referencia bibliográfica: es el conjunto mínimo de datos que permite la
identificación de un
estudio, tales como
su autor, código, año y título. El Reporte de Evaluación debe incluir la
referencia bibliográfica de los estudios que se indican en el anexo III.1.A.
Legajo Técnico de este reglamento.
Registro: es el acto administrativo mediante el que la AC aprueba la venta y
utilización de un IAGT, en los términos previstos en el presente reglamento.
Registrante: es la persona física o jurídica que solicita el registro de un IAGT a la
AC.
Reporte (s) de evaluación: reporte oficial, monografía o documento
mediante el cual la Autoridad reguladora de un país miembro de la OCDE o de un
país adherente pleno al sistema de AMD de esa organización, integra y aprueba
los resultados y referencias bibliográficas de todos los informes de pruebas,
estudios y otra información relevante presentada por quien solicita la
aprobación de un IAGT.
Residuo: es cualquier sustancia específica presente en alimentos, productos
agrícolas o alimentos para animales, como consecuencia del uso de plaguicidas.
El término incluye cualquier derivado de un plaguicida, ingrediente activo,
productos de conversión, metabolitos y productos de reacción y las impurezas
consideradas de importancia toxicológicas.
Sistema de Aceptación Mutua de Datos (AMD) de la OCDE: es un acuerdo
multilateral integrado por tres instrumentos de la OCDE: i) la Decisión del
Consejo sobre la Aceptación Mutua de Datos en la Evaluación de Químicos de 1981
(revisada en 1997); ii) la Decisión - Recomendación del Consejo sobre el
Cumplimiento con los Principios de Buenas Prácticas de Laboratorio de 1989 y,
iii) la Decisión del Consejo sobre la Adhesión de países No Miembros a los
Actos del Consejo relacionados con la Aceptación Mutua de Datos en la
Evaluación de Sustancias Químicas de 1997.
Titular de registro: es la persona física o jurídica propietaria del
registro de un IAGT ante la AC.
Titular de la información:
persona física o jurídica que ostenta un derecho de propiedad sobre la
información presentada para el registro, y por ende puede controlar y disponer
respecto de esta.
(Así
adicionada la definición anterior por el artículo 2° del decreto ejecutivo N°
43563 del 28 de mayo de 2022)
Vehículo físico que contiene IAGT: medio inerte que proporciona la adecuada
superficie de contacto o que se utiliza como soporte de un IAGT.
Ficha articulo
Artículo 4. Símbolos y abreviaturas. Para los efectos de este Reglamento se
entenderá por:
AC: Autoridad Competente.
AMD: Aceptación Mutua de Datos de la OCDE.
APVMA: Autoridad Australiana de Plaguicidas y Medicamentos Veterinarios
(Australian Pesticides and Veterinary Medicines Authority).
BVL: Oficina Federal de Protección al Consumidor y Seguridad
Alimentaria, Alemania (Federal Office of Consumer Protection and Food Safety,
Alemania).
CAS: Número de identificación química (por sus siglas en inglés).
EFSA: La Autoridad Europea para la Seguridad de los Alimentos (European
Food Safety Authority).
EPA: Agencia de Protección Ambiental (Environmental Protection Agency
United States).
FAO: Organización de las Naciones Unidas para la Agricultura y la
Alimentación (por sus siglas en inglés).
IAGT: Ingrediente activo grado técnico.
ISO: Organización Internacional de Normalización.
IUPAC: Unión Internacional de Química Pura y Aplicada (por sus siglas en
inglés).
MAG: Ministerio de Agricultura y Ganadería.
MINAE: Ministerio de Ambiente y Energía.
MINSA: Ministerio de Salud.
OCDE: Organización para la Cooperación y el Desarrollo Económicos.
OMS: Organización Mundial de la Salud.
SFE: Servicio Fitosanitario del Estado.
TC: Material Técnico.
TK: Concentrado Técnico.
Ficha articulo
Artículo 5. Administración del Registro. El registro de IAGT
será administrado por el SFE, el cual, para los efectos de aplicación e
interpretación del presente reglamento, será la AC. El MINSA y el MINAE
participarán como autoridades revisoras en las etapas del proceso de registro
que se indicarán, de acuerdo con sus competencias legales.
Ficha articulo
Artículo 6. Alcances de la solicitud de registro. Con esta modalidad
podrán registrarse los IAGT aprobados o registrados en un país miembro de la
OCDE o en un país adherente pleno del sistema de AMD de esa organización. Lo
anterior, siempre que ese IAGT tenga la misma concentración mínima y provenga
del mismo origen y fabricante que fue evaluado y aprobado o registrado en tales
países.
La información que se presente por parte del registrante deberá ser la
que sustentó o dio origen a la aprobación o registro en el país miembro de la
OCDE o en el país adherente pleno del sistema de AMD, y contener, al menos, la
información que se indica en el Anexo III de este decreto. Por lo tanto, cada
solicitud de registro será válida únicamente para un producto o fabricante;
cada IAGT del mismo fabricante tendrá un único titular.
Ficha articulo
Artículo 7. Material de Referencia Certificado de IAGT y sustancias
relacionadas solicitadas en el programa de monitoreo de control de residuos. La AC cuenta con la facultad
de solicitar que los registrantes entreguen Material de Referencia Certificado
de las sustancias que incluye la definición de residuo adoptada por Costa Rica
para el Ingrediente activo, y de las impurezas relevantes, en caso de estar
presentes.
El Material de Referencia Certificado deberá cumplir los lineamientos de
la norma internacional ISO 17034 en su versión vigente y deberá venir
acompañado de la documentación, incertidumbre y trazabilidad que especifica la
norma, en envase sellado y con fecha de caducidad vigente. El Material de
referencia certificado podrá ser suministrado por el fabricante o instituciones
estándar o compañías que venden sustancias de referencia. En caso de que el
Material de referencia certificado no se encuentre disponible en el mercado se permitirá
la entrega de patrones analíticos elaborados por el fabricante bajo los
lineamientos de las Buenas Prácticas de Laboratorio establecidas por la OCDE.
Los registrantes aportarán el estándar y las muestras previa justificación
técnica de la AC.
Ficha articulo
Artículo 8. Posibilidad de examinar los registros aprobados de IAGT. Las Autoridades revisoras
competentes podrán examinar de oficio o por solicitud de terceros justificada
técnica y científicamente, los registros aprobados del IAGT, en los siguientes
casos:
a) Cuando se conozca información que no se haya considerado como un
requisito durante la evaluación que otorgó el registro o fuere posterior a
éste, y que sea de importancia para salvaguardar la salud, el ambiente y la
agricultura.
b) Cuando cualquier información que se encuentra en el expediente de
registro, haya sido modificada o actualizada y que ésta sea indispensable para
sustentarlo.
c) Cuando en el país donde se otorgó la autorización o el registro del
IAGT, se haya tomado la decisión de prohibir o restringir el plaguicida por
afectar la salud humana, el medio ambiente o la agricultura, aun cuando el
producto esté siendo utilizado conforme a lo aprobado. Para esta determinación
se realizará un análisis basado en información técnica y científica, la que
podrá ser requerida por la AC o las Autoridades revisoras competentes.
Para todo lo anterior, las Autoridades revisoras competentes podrán
requerir información o análisis adicionales y documentación de apoyo durante la
vigencia del registro.
Ficha articulo
Artículo 9. Uso del registro como perfil de referencia. La AC queda
facultada para utilizar el registro por esta modalidad como perfil de
referencia en los procesos de registro bajo modalidad de equivalencia, aunque
posteriormente el registro se cancele a solicitud del titular o expire el plazo
de vigencia sin que se haya renovado, en el tanto el IAGT permanezca vigente en
el país de donde se aprobó o registró.
Ficha articulo
Artículo 10. Reconocimiento
de la evaluación aprobada de los estudios técnicos. Las
Autoridades Revisoras competentes reconocerán las evaluaciones de los
estudios técnicos señalados en el punto I del Anexo III del presente reglamento y que
son requeridos para el registro de IAGT data completa, realizadas por las autoridades
reguladoras de los países miembros de la OCDE y de los países adherentes
al Sistema de Aceptación Mutua de Datos (AMD) de la OCDE, para la aprobación
de un IAGT cuyo registro se solicite en nuestro país, siempre y cuando dichos
estudios hayan sido aprobados por algún(os) país(es) miembro(s) de OCDE o
algún(os) país(es) adherentes al sistema AMD de la OCDE de acuerdo a lo que señala
el Reporte de evaluación.
El IAGT que es objeto de
registro en Costa Rica mediante este mecanismo debe estar registrado o aprobado
en algún(os) país(es) OCDE o en algún(os) país(es) adherentes al sistema AMD de
la OCDE que realizó las evaluaciones del IAGT.
(Así
reformado por el artículo 1° del decreto ejecutivo N° 43563 del 28 de mayo de
2022)
Ficha articulo
Artículo 11. Etiquetado. En relación con el etiquetado se aplicará el
Reglamento Técnico Centroamericano RTCA 65.05.67:18 Insumos Agrícolas.
Ingrediente activo grado técnico, plaguicidas químicos formulados, sustancias
afines, coadyuvantes y vehículos físicos de uso agrícola; así como los
requisitos para la elaboración de etiquetas y panfletos, definidos en la Resolución
N° 401-2018 (COMIECO-LXXXIII), Decreto Ejecutivo N° 41400-COMEXMEIC-MAG,
publicado en el Diario Oficial La Gaceta No. 218 del 23 de noviembre de 2018 o
la normativa que se encuentre vigente.
Ficha articulo
Capítulo II
Sobre el régimen de protección a los datos de prueba
Artículo 12. Régimen de protección a los datos de prueba. La protección a los
datos de prueba, de conformidad con lo establecido en este Reglamento, en la
Ley de Información No Divulgada, Ley N° 7975 del 4 de enero del 2000, y el
Reglamento a la Ley de Información No Divulgada, Decreto Ejecutivo N°
34927-J-COMEX-S-MAG, será aplicable a los productos agroquímicos nuevos, tal
como se definen en este Reglamento.
En consecuencia, no se otorgará protección para aquel IAGT que contiene
una entidad química que se encuentre en un registro que se haya otorgado
previamente en Costa Rica, como IAGT o formando parte de un plaguicida
sintético formulado o vehículo físico.
La AC prevendrá que terceros sin autorización del registrante o del
titular del registro con datos de prueba protegidos, usen y accedan a dicha
información durante la vigencia del plazo de protección de diez años,
establecido por el artículo 16 del Reglamento a la Ley de Información No
Divulgada Nº 34927-J-COMEX-S-MAG. El personal afecto a los procedimientos de registro
deberá abstenerse de revelar, sin autorización del registrante o del titular
del registro, los datos de prueba, excepto cuando sea necesario para proteger
el interés público, la salud pública y al ambiente, y se protejan los datos de
prueba contra su uso comercial desleal.
Mientras esté vigente la protección de los datos de prueba en el
expediente, esta información no podrá ser utilizada por otros registrantes para
sustentar sus registros, salvo que el titular del derecho lo autorice. Una vez
vencido el plazo de protección, no se requiere autorización del titular del
derecho para sustentar el registro para la modalidad de registro por
equivalencia.
Ficha articulo
Artículo 13. Uso del Registro como perfil de referencia. La AC podrá
utilizar en cualquier momento el registro como perfil de referencia sin que
tenga que solicitar la autorización del registrante, salvo en aquellos casos
que se encuentre con protección de datos de prueba.
Ficha articulo
Artículo 14. Requisitos para aplicar el régimen de protección a los
datos de prueba. Todo registrante de un producto agroquímico nuevo que solicite
protección de datos de prueba que cumplan con las disposiciones legales y
reglamentarias, deberá presentar una declaración jurada protocolizada rendida
ante Notario Público, suscrita por el registrante o su representante legal en
donde indique:
1) el IAGT para el que se solicita el registro indicando el nombre común
y químico según IUPAC, número de identificación CAS. En caso de que no esté
disponible el número de identificación CAS la empresa deberá justificarlo.
2) los datos de prueba que sustentan el registro del IAGT contenidos en
la solicitud; con la indicación de si el registrante: i) generó los datos de
prueba; ii) obtuvo los derechos sobre dichos datos de prueba; o bien iii) está
autorizado por otro registrante o por el titular del registro para usarlos,
según sea el caso.
Ficha articulo
Artículo 15. Limitaciones. Con el fin de asegurar la protección de los
datos de prueba, la AC no permitirá el uso de datos de prueba con protección
vigente como evidencia o información de apoyo para el registro por parte de un
registrante diferente al titular del registro, a menos que éste haya autorizado
por escrito el uso de dichos datos de prueba.
Ficha articulo
Artículo 16. Análisis de la petición de protección de datos. Cuando el
registrante solicite la protección de datos de prueba, la AC verificará que se
trata de un producto agroquímico nuevo que no se encuentre en un registro que
se haya otorgado previamente en Costa Rica, como IAGT o formando parte de un
plaguicida sintético formulado o vehículo físico, y lo incluirá en una lista de
IAGT nuevos, a los que se otorgue un registro indicando:
1) número de registro,
2) modalidad de registro,
3) nombre con el que está registrado,
4) nombre del titular,
5) fecha de inicio y de expiración del plazo de protección de datos de
prueba.
Ficha articulo
Artículo 17. Publicidad y plazo de protección de datos. El plazo de
protección de datos de prueba será de diez años a partir de la fecha de
aprobación del registro por parte de la AC. La AC pondrá a disposición del
público el listado de productos agroquímicos con protección de datos de prueba,
indicando el nombre del IAGT protegido, nombre del titular, fecha de inicio y expiración
de la protección.
Asimismo, la AC mantendrá para su uso exclusivo, un listado de los datos
de prueba objeto de protección, identificando claramente el tipo de estudio, la
fecha y sitio donde se desarrolló, así como el número del estudio y su
patrocinador.
Durante el plazo de protección de los datos de prueba, solo su titular o
un registrante con autorización escrita del titular podrán hacer uso de estos
para verificar un nuevo registro. Al expirar el plazo de protección de los
datos de prueba, la AC podrá autorizar registros, al amparo de los datos de
prueba generados por un sujeto distinto al registrante, sin necesidad de una autorización
del titular de esos datos de prueba.
Ficha articulo
Capítulo III
Procedimiento para optar por el registro de IAGT por reconocimiento de
la aprobación
de evaluaciones de estudios técnicos de las autoridades reguladoras de
los países
miembros de la OCDE o de las autoridades reguladoras de los países adherentes
al
sistema de AMD de esa organización.
Artículo 18. Solicitud de
registro de IAGT y requisitos aplicables. El IAGT que se
pretenda registrar mediante la aplicación de este reglamento debe provenir de
la misma empresa o titular de la información y tener la misma concentración mínima
que el IAGT aprobado por la Autoridad Reguladora.
El interesado en solicitar
el registro de IAGT mediante el reconocimiento de la evaluación de los estudios
técnicos realizada por la Autoridad Reguladora debe presentar su solicitud ante
la unidad que administra el registro en el SFE, a través del formulario visible
en el Anexo I del presente reglamento y cumplir con los siguientes requisitos:
a) Presentar debidamente
completo el formulario de solicitud de registro IAGT (Anexo I del presente
reglamento), en cada uno de sus apartados.
b) Presentar los estudios,
documentos o certificados correspondientes al legajo de información
administrativa y legajo de información confidencial señalados en el apartado II
del Anexo III del presente reglamento. Dichos estudios e información deben
suministrarse por medio de datos provenientes de ensayos o estudios realizados
sobre el producto que se quiere registrar y deben ser los mismos que sustentaron
la aprobación en el país miembro de la OCDE o en el país adherente del
sistema de AMD de esa organización. En caso de que se cuente con estudios de la
misma empresa y titular de la información, elaborados en planta piloto y de diferente
origen al que se quiere registrar, podrán ser aceptados para reconocimiento en el
caso de los estudios toxicológicos, eco toxicológicos, destino ambiental y las propiedades
fisicoquímicas que aplican para el IAGT puro, previa justificación técnica
razonada por parte del registrante.
En caso de haberse emitido
en un idioma diferente al español o al inglés, deberá presentarse una
traducción al español.
c) Aportar el Reporte (s)
de Evaluación emitido por la Autoridad reguladora, el cual deberá contener las
evaluaciones y aprobaciones de los estudios y requisitos enumerados en el
legajo de información técnica del apartado I.A del Anexo III del presente
reglamento. En caso de que el informe de evaluación no contemple algunos de los
requisitos solicitados en el Anexo III se podrá permitir la presentación del
informe o reporte de evaluación de otros países OCDE o países adherentes del
sistema AMD de esa organización donde conste la aprobación de los estudios,
siempre y cuando correspondan al mismo origen, concentración y fabricante.
Además, si la Autoridad
Reguladora en su informe no emite un reporte de evaluación tal y como se
especifica anteriormente, se aceptará junto con el reporte de evaluación un
informe hecho por el registrante detallando los resultados y referencias
bibliográficas de todos los informes de pruebas, estudios y otra información
relevante que presentaron ante la autoridad reguladora y que dicho informe
venga avalado por la Autoridad Reguladora.
Si el reporte de evaluación
o el informe fue emitido en un idioma diferente al español o al inglés, deberá
presentarse una traducción oficial al idioma español.
Se hace el reconocimiento
de la evaluación de los datos técnicos contenidos en el Reporte
de Evaluación o el informe, con el fin de comprobar que el IAGT no afecta la
salud y el ambiente. Dicha evaluación es realizada por las Autoridades
revisoras competentes según sus competencias legales.
d) Estar al día en todas
sus obligaciones obrero-patronales con la Caja Costarricense de Seguro Social y
Fondo de Desarrollo y Asignaciones Familiares (FODESAF), situación que será
verificada por la AC mediante consulta en la oficina virtual correspondiente.
e) Presentar copia de los
estudios indicados en el anexo III.1.A. Legajo Técnico del presente reglamento,
que fueron presentados a la Autoridad Reguladora del país OCDE o país adherente
pleno del sistema de AMD de esa organización, que aprobó o registró el IAGT y
cuyos datos constan en el Repo1ie (s) de evaluación o el informe señalado(s) en
el punto c de este artículo. La información que se presente deberá ser la misma
que sustentó o dio origen al registro o autorización en el o los países(es)
miembro(s) de OCDE o país(es) adherente(s) del sistema de AMD de esa
organización. En caso de haberse emitido en un idioma diferente al español o al
inglés, deberá presentarse una traducción al idioma español.
f) Presentar la declaración
jurada indicada en el Anexo II del presente reglamento.
g) Indicar si existe una
solicitud de registro de IAGT bajo la modalidad de data completa pendiente de
resolución ante el Servicio Fitosanitario del Estado, para la misma entidad
química. En estos casos deberá indicar el número de trámite.
h) Presentar el formulario
previsto en el anexo IV del presente reglamento, denominado "Formulario
de recopilación de datos técnicos del Reporte de Evaluación."
(Así
reformado por el artículo 1° del decreto ejecutivo N° 43563 del 28 de mayo de
2022)
Ficha articulo
Artículo 19. Conformación del expediente administrativo. Desde la
presentación de la solicitud inicial y luego de dictada la resolución final, la
AC, debe mantener los expedientes relativos a las solicitudes de registro,
debidamente ordenados y foliados, sin perjuicio de los expedientes internos que
elabore cada Autoridad revisora competente.
Ficha articulo
Artículo 20. Medio electrónico permanente. El registrante debe
designar una dirección de correo electrónico como el medio para la recepción de
notificaciones relacionadas con el trámite de registro. La seguridad de la
cuenta designada es responsabilidad del registrante.
El medio electrónico podrá ser modificado por el registrante en
cualquier tiempo, sin perjuicio de las consecuencias jurídicas surgidas hasta
ese momento producto de las notificaciones efectuadas al medio electrónico
permanente anteriormente señalado.
Ficha articulo
Artículo 21. Trámite de admisibilidad. La AC, dentro del
plazo máximo de 8 días hábiles contados a partir de la presentación de la
solicitud de registro, debe realizar una revisión de admisibilidad de la
solicitud, que consistirá en una verificación de forma de los requisitos definidos
en el artículo 18 del presente reglamento, de acuerdo con lo establecido en la Guía
de Admisibilidad publicada en la página web de la AC.
Una vez finalizado el proceso de admisibilidad y si se determina que el
trámite fue admitido, la solicitud de registro se tramitará en los términos
previstos en este reglamento.
La verificación del contenido de los requisitos documentales y técnicos
corresponderá a las autoridades revisoras competentes.
Ficha articulo
Artículo 22. Prevención única. Dentro del plazo anterior, la AC debe
prevenir por una única vez al registrante la presentación de cualquier
documento faltante o la subsanación de cualquier requisito documental o técnico
establecido, relativo a la solicitud de registro, otorgándole al efecto un plazo
de 20 días hábiles para cumplir con los aspectos prevenidos, plazo que podrá prorrogarse
por 10 días hábiles adicionales y por una única vez a solicitud del
registrante.
Tal prevención se realizará con base en la verificación de requisitos
previstos en el artículo 18 del presente reglamento, sin que puedan
establecerse otros requisitos diferentes a los contemplados ahí, las cuales
estarán a disposición en el sitio Web de la AC.
Una vez cumplida la prevención por el registrante, la AC cuenta con un
plazo de 5 días hábiles para revisar la respuesta aportada y determinar si el
registrante cumplió con cada uno de los aspectos prevenidos.
Ficha articulo
Artículo 23. Archivo de la gestión en etapa de admisibilidad. Vencido el plazo
señalado en el artículo anterior, si la AC verifica que los incumplimientos o
inconsistencias originales no fueron acatados en su totalidad, ordenará el
archivo definitivo de la gestión, acto que debe comunicársele al registrante de
conformidad con lo previsto en el artículo 264 de la Ley General de la
Administración Pública. Esta resolución tendrá los recursos ordinarios y
extraordinarios contemplados en la Ley General de la Administración Pública.
Ficha articulo
Artículo 24. Evaluación técnica ante las Autoridades revisoras
competentes. El MINSA, el MINAE, así como las dependencias competentes del SFE,
evaluarán, según sus competencias técnicas la documentación e información
administrativa, técnica y confidencial aportada en la solicitud de registro.
Ficha articulo
Artículo 25. Solicitud de aclaración o adición de información técnica. Como parte del proceso
de evaluación técnica, cada una de las Autoridades revisoras competentes tienen
la facultad de solicitar, por una única vez y de manera justificada,
aclaraciones e información técnica adicional a la aportada en la solicitud de
registro, siempre y cuando esta información resulte imprescindible para poder
realizar el análisis de fondo de la solicitud y por ende, verificar que el
producto no afecta la salud, el ambiente o el patrimonio fitosanitario, y sin
que esto implique establecer requisitos adicionales a los requeridos
previamente. Para tales efectos, se le otorgará al registrante un plazo de 10
días hábiles, el cual podrá prorrogarse a solicitud expresa de éste por una
única vez y por un plazo adicional igual.
Asimismo, las autoridades revisoras cuentan con un plazo adicional de 10
días hábiles para
revisar la respuesta
aportada por el registrante.
Vencido el plazo anterior, si el registrante no presentó la información
o aclaraciones requeridas, o bien no cumplió con la presentación de la
totalidad de la información en los términos requeridos, se declarará sin
derecho al correspondiente trámite, conforme con lo previsto en el artículo 264
de la Ley General de la Administración Pública. Esta resolución tendrá los
recursos ordinarios y extraordinarios contemplados en la Ley General de la
Administración Pública. La Autoridad revisora competente debe comunicar al
registrante y a la AC la resolución correspondiente para su incorporación en el
expediente respectivo.
Ficha articulo
Artículo 26. Procedimiento de evaluación técnica de la solicitud de
registro de IAGT de
los estudios
presentados y el reporte de evaluación. Una vez que se ha determinado que la solicitud
cumple con el proceso de admisibilidad previsto en el artículo 21 del presente reglamento,
se procederá en los términos que se indican a continuación:
El análisis de la información técnica se realizará de conformidad con lo
solicitado en el artículo 18 del presente reglamento, cumpliendo el siguiente
orden:
1. Análisis químico.
2. Análisis toxicológico, ecotoxicológico y de destino ambiental de
forma simultánea.
3. Análisis agronómico.
La solicitud se trasladará a la dependencia competente de la AC para el
análisis de los aspectos químicos. Para tales efectos, el revisor cuenta con un
plazo de 17 días hábiles para realizar el análisis químico que corresponde al
análisis de los requisitos señalados en el Anexo III del presente reglamento,
correspondientes a los estudios del Legajo Confidencial, información del Legajo
Administrativo y Legajo Técnico - Reporte de evaluación.
Una vez realizado dicho análisis, y si el informe es positivo, se debe
emitir el informe químico de reconocimiento de la evaluación de los estudios
técnicos y la evaluación correspondiente al legajo confidencial y administrativo,
el que debe ser trasladado a la unidad que administra el registro de la AC,
quien deberá comunicarle al registrante en el día hábil siguiente a la fecha de
emisión. En caso de que el informe sea negativo se procederá con el archivo
definitivo del trámite, previa emisión de una resolución final para denegar la
solicitud de registro. Lo anterior sin perjuicio de los recursos
administrativos que correspondan contra el acto denegatorio según lo
establecido sobre la materia en la Ley General de la Administración Pública.
Una vez incorporado el informe químico de aprobación en el expediente,
la AC trasladará simultáneamente la solicitud de registro a las dependencias
competentes del MINSA y del MINAE, lo anterior en el plazo de un día hábil.
Dentro del plazo de 10 días hábiles, ambas instituciones realizarán la
evaluación técnica de la información presentada, para el reconocimiento de la
evaluación de los estudios técnicos, la revisión de los documentos del legajo
administrativo y el análisis sobre la salud humana y el ambiente, según su
competencia. Una vez finalizado dicho plazo se debe emitir el informe de evaluación
técnica correspondiente, que deberá ser comunicado a la AC y notificado al registrante
en el día hábil siguiente a la fecha de emisión. En caso de que el informe sea
negativo por parte de alguna de las autoridades revisoras competentes de MINSA
o MINAE, se procederá con el archivo definitivo del trámite, previa emisión de
una resolución final para denegar la solicitud de registro, por parte de la
autoridad revisora competente de MINSA o MINAE. Lo anterior sin perjuicio de
los recursos administrativos que correspondan contra el acto denegatorio según
lo establecido sobre la materia en la Ley General de la Administración Pública.
Cuando el registrante reciba los informes con criterio positivo de la
parte química, ecotoxicológica y toxicológica, tendrá 3 días hábiles para
presentar al SFE la etiqueta y la hoja de seguridad con las observaciones
indicadas en cada uno de los informes, para poder continuar con la última etapa
de evaluación, que sería la agronómica. Finalizado el plazo anterior, la AC trasladará
la solicitud a su dependencia competente con el objetivo de continuar con la
última etapa de revisión técnica, correspondiente al análisis agronómico.
Para tales efectos, la dependencia competente de la AC cuenta con un
plazo de 5 días hábiles para realizar el análisis agronómico. Una vez
finalizado dicho plazo se debe emitir el informe de evaluación técnica
correspondiente, el cual debe ser comunicado a la AC y notificado al registrante
en el día hábil siguiente a la fecha de emisión. En caso de que el informe sea
negativo se procederá con el archivo definitivo del trámite, previa emisión de
una resolución final para denegar la solicitud de registro. Lo anterior sin
perjuicio de los recursos administrativos que correspondan contra el acto
denegatorio según lo establecido sobre la materia en la Ley General de la
Administración Pública.
Una vez que han sido trasladados los informes señalados a la AC, emitirá
la resolución de registro en los términos que se indican en el artículo
siguiente.
Ficha articulo
Artículo 27. Resolución de aprobación. Una vez finalizado
el proceso de evaluación técnica de las solicitudes por parte de las
Autoridades revisoras competentes y emitidos los informes positivos,
correspondientes, la AC dictará la resolución de aprobación en el plazo máximo
de 4 días hábiles, acto que será emitido y comunicado al registrante en el
plazo máximo de 1 día hábil a partir de la emisión de dicha resolución.
Ficha articulo
Artículo 28. Vigencia y renovación del registro. Los registros
tendrán una vigencia de 10 años a partir de su inscripción. Dentro de los 6
meses antes de su vencimiento, el registrante deberá presentar la solicitud de
renovación del registro previa presentación de los requisitos que se indican a
continuación:
1. Formulario de renovación del registro, firmado por el titular del
registro o su representante, en la que debe indicar el número de registro
objeto de renovación (Anexo I).
2. Comprobante de pago del arancel vigente.
3. Certificado de análisis del IAGT con menos de 1 año de haber sido
emitido, original o autenticado por un notario público. Dicho certificado debe
incluir la fecha de análisis, número de lote utilizado en el análisis y
fabricante del IAGT.
4. Certificado de composición cualitativa cuantitativa del IAGT emitido
por la casa matriz o por el fabricante y firmado por el profesional
responsable, con menos de 1 año de haber sido emitido. Se debe indicar la
identidad del ingrediente activo, impurezas y aditivos (éste último cuando
corresponda y aplique al caso concreto) de acuerdo con su nombre químico según
IUPAC y el número CAS cuando estén disponibles; en caso de no estar disponible,
se debe presentar la estructura química. Se deberá presentar firmado en
original, el cual contendrá:
a. Concentración mínima del IAGT expresado en porcentaje m/m (o g/kg) o porcentaje
m/v. En el caso de indicarse la concentración en m/v debe declararse la
densidad.
b. Concentración máxima de cada impureza mayor o igual a un gramo por kilogramo
(1 g/kg) ó 0,1%m/m.
c. Concentración máxima de impurezas relevantes y en caso de no estar
presentes se deberá indicar la no presencia de las mismas.
d. Concentración mínima y máxima de otros aditivos presentes, expresados
en g/kg ó porcentaje, cuando corresponda y aplique al caso concreto. Debe
indicar la función (por ejemplo, estabilizante).
e. En caso de que el ingrediente activo sea un TK, deberá presentarse
los límites máximo y mínimo del ingrediente activo y la concentración en base
seca.
Así mismo, la renovación procede si se cumplen todas las siguientes
disposiciones:
1. La concentración del IAGT reportada en el certificado de composición
es igual o mayor a la concentración mínima registrada.
2. No se presentan nuevas impurezas.
3. No se incrementan los límites de impurezas relevantes tal cual lo
certifica la especificación registrada.
4. Los límites certificados para todas las impurezas no-relevantes, tal
cual han sido certificados en la especificación registrada, no deben excederse
más allá de los siguientes niveles:
|
Límites certificados de impurezas no- relevantes en las especificaciones técnicas de la
especificación registrada
|
Incremento máximo aceptable
|
|
< 6 g/kg
|
3 g/kg
|
|
>6 g/kg
|
50% del
límite certificado
|
La AC deberá resolver la solicitud de renovación del registro en un
plazo de 15 días hábiles mediante resolución administrativa, que se agregará al
expediente respectivo.
Los registros vigentes que no presenten la solicitud de renovación serán
cancelados sin más trámite que el dictado de una resolución donde se haga
constar que el mismo no fue renovado.
El registro se considerará vigente durante el tiempo en que la AC
resuelva la solicitud de renovación.
No obstante, lo anterior, los registros otorgados pueden ser cancelados,
en cualquier momento por la AC, por cualquiera de las causales establecidas en
este reglamento o a solicitud del titular y previa apertura de un procedimiento
administrativo de cancelación de registro.
Ficha articulo
Artículo 29. Suspensión del registro IAGT. La AC suspenderá el
registro si concurren una o más de las siguientes causales:
a) El titular de registro no proporcione en el plazo otorgado por la AC,
la información requerida.
b) Por orden de la autoridad judicial, ambiental o sanitaria notificada
a la AC por la autoridad que ordena el acto de suspensión.
c) Cuando el titular del registro no se encuentre al día en el pago del
canon.
d) Cuando el titular del registro no proporcione en el plazo otorgado
por la AC el material de Referencia Certificado de IAGT y sustancias
relacionadas.
La suspensión del registro, otorgado en cualquiera de sus modalidades,
impide, durante el período de suspensión, el uso y comercialización en el país
del producto registrado. Tampoco se podrá formular, reformular, importar,
envasar, reenvasar, o reempacar los productos, a excepción que estas acciones
sean necesarias para corregir la causal por la que se suspendió el registro.
La AC, ordenará la suspensión de registro mediante el dictado de una
resolución sustentada técnica y legalmente, con indicación del motivo que la
origina, y se mantendrá hasta tanto se corrija el motivo de la suspensión. No
obstante, si tal corrección no se ha realizado dentro de un plazo de seis
meses, a partir de su notificación se procederá a la cancelación del registro
de conformidad con el artículo 30, a excepción de aquellas suspensiones
ordenadas por la instancia judicial.
Ficha articulo
Artículo 30. Cancelación de registro IAGT. La AC cancelará el
registro de un IAGT, siguiendo el debido proceso, si concurren una o más de
causales que se indican a continuación:
a) Por solicitud expresa el registrante.
b) Cuando el registro haya sido otorgado con vicios de nulidad absoluta,
evidente y manifiesta y no haya cumplido con requisitos que se señalan en este
reglamento.
c) Cuando las Autoridades revisoras competentes determinen que el
producto, aún utilizado bajo las recomendaciones de uso, representa un riesgo
inaceptable para la salud, el ambiente y agricultura.
d) Cuando el titular del registro no haya solicitado la renovación del
registro y expire el plazo de vigencia del registro.
e) Cuando la AC demuestre que la información rendida bajo juramento no
coincide con lo declarado.
f) Cuando el IAGT registrado es cancelado o desautorizado por la
autoridad reguladora del país OCDE o del país adherente pleno del sistema de
AMD de esa organización, por razones de afectación a la salud o el ambiente,
previa valoración científica de las Autoridades revisoras competentes.
g) Cuando las causas que dieron motivo a la suspensión del registro no
se subsanen en el plazo conferido por la AC.
h) Cuando el Codex alimentarius, la EPA o EFSA eliminen para todos los
usos autorizados, el límite máximo de residuos (LMR) adoptado en Costa Rica
según la normativa correspondiente, para los productos que utilicen el IAGT
registrado.
Ficha articulo
Artículo 31. Información sobre el registro de acceso público. La siguiente
información es considerada de acceso público.
1. La AC mantendrá actualizada y a disposición del público a través de
su página Web o de algún otro medio tecnológico oficial la siguiente
información:
a) Lista de los IAGT registrados mediante la aplicación de este
reglamento
b) La información sobre personas físicas o jurídicas inscritas ante la
AC y con registro vigente.
c) La lista de IAGT con protección de datos de prueba, indicando número
de registro, nombre con el que está registrado, nombre del titular, fecha de
inicio y expiración de la protección.
d) La lista de los países miembros de la OCDE y de los países adherentes
plenos del sistema de AMD de esa organización, las entidades competentes de la aprobación
de IAGT y la información de contacto.
2. Los sujetos que requieran la siguiente información, deberán hacerlo
mediante nota, la que será registrada y archivada, salvo los funcionarios públicos
autorizados.
a) Un Reporte en el que se incluya los datos técnicos del IAGT de acceso
público y la decisión de la AC. Para tales efectos se recomienda a manera de
referencia, el formato de la Guía de la OCDE para la elaboración de Reportes de
Evaluación de Datos de Productos de Protección de las Plantas y sus Sustancias
Activas, revisión 3, de abril de 2008, o revisiones posteriores.
b) La hoja de datos de seguridad.
c) La etiqueta aprobada.
d) Método de análisis del ingrediente activo.
e) Método de análisis de residuos.
f) Método de análisis de las impurezas relevantes.
g) La tolerancia máxima de las impurezas relevantes del ingrediente
activo grado técnico.
Ficha articulo
Disposiciones transitorias
TRANSITORIO PRIMERO. - Las solicitudes de Registro de IAGT en la modalidad
de data completa pendientes ante el Servicio Fitosanitario del Estado, en el
momento de entrar en vigencia este Decreto Ejecutivo, podrán continuar con la
normativa vigente a su presentación.
Ficha articulo
TRANSITORIO SEGUNDO. - Las personas jurídicas o físicas con solicitudes
de Registro de IAGT en la modalidad de data completa pendientes de resolución
ante el Servicio Fitosanitario del Estado, bajo los Decretos Ejecutivos N°
33495-MAG-S-MINAE-MEIC y N° 40059- MAG-MINAE-S, podrán acogerse al proceso de
trámite establecido en el presente reglamento. Para tales efectos, deberán
presentar una nueva solicitud de registro cumpliendo con la totalidad de los
requisitos establecidos en el presente reglamento y serán tramitados en el
orden que han sido presentados bajo esta modalidad.
En estos casos y para todos los efectos, las solicitudes presentadas
bajo los Decretos Ejecutivos N° 33495-MAG-S-MINAE-MEIC y N° 40059- MAG-MINAE-S,
quedarán suspendidas en su tramitación hasta que se resuelva la solicitud bajo
los lineamientos previstos en el presente reglamento. En el caso que la
solicitud de registro sea aprobada, se procederá a la cancelación de las
solicitudes pendientes de resolución bajo los decretos ejecutivos indicados,
salvo que el solicitante indique, en un plazo máximo de 10 días hábiles,
expresamente que desea continuar con su tramitación.
Ficha articulo
Artículo 32. Vigencia. Rige a partir de su publicación en el Diario
Oficial La Gaceta.
Dado en la Presidencia de la República, en la ciudad de San José, a los
veintiséis días del mes de enero del año dos mil veintiuno.
Ficha articulo
ANEXO I
FORMULARIO DE SOLICITUD REGISTRO DE INGREDIENTE ACTIVO POR
RECONOCIMIENTO DE LA EVALUACIÓN APROBADA DE LOS ESTUDIOS
TÉCNICOS POR PARTE DE LAS AUTORIDADES REGULADORAS DE LOS
PAÍSES MIEMBROS DE LA OCDE O DE LAS AUTORIDADES REGULADORAS
DE LOS PAÍSES ADHERENTES DEL SISTEMA DE ACEPTACIÓN MUTUA DE
DATOS DE ESA
ORGANIZACIÓN
|
1. Información
general sobre la solicitud
|
|
1.1 Motivo
de la solicitud:
|
|
( ) Registro nuevo IAGT data
completa por reconocimiento de la evaluación aprobada de los estudio técnicos por parte
de las autoridades reguladoras de los países
miembros de la OCDE o de las autoridades reguladoras de los países
adherentes del sistema
de aceptación mutua de datos de esa organización.
|
( ) Renovación de IAGT data completa por reconocimiento de la evaluación aprobada de los estudios técnicos por parte
de las autoridades regulatorias de los países miembros de la OCDE o de las autoridades reguladoras de los países adherentes del sistema de aceptación mutua de datos de esa organización. Se debe
indicar el número
de registro.
|
|
1.2 Sobre
el registrante
|
|
Número de registro de la empresa:
|
Nombre o razón social (persona física
o jurídica):
|
|
1.3 Sobre
el representante legal
|
|
Nombre completo:
|
Número de cédula:
|
|
2. Datos
del producto:
|
|
2.1 Nombre común o genérico, propuesto o aceptado por ISO por sus siglas
en inglés, de no existir
éste aportar el utilizado por IUPAC o el propuesto por la Convención Chemical Abstract, o por último el propuesto por el fabricante:
|
2.2 Nombre del producto o marca
comercial:
|
2.3 Número CAS
|
|
2.4 Masa molecular
|
2.5 Sinónimos:
|
2.6 Fórmula
molecular
|
|
2.7 Clase
|
2.8 Grupo químico IUPAC:
|
2.9 Número CIPAC:
|
|
2.10 Concentración mínima del IAGT:
|
|
2.11 Concentración máxima de impurezas relevantes a partir
de su límite de
detección:
|
|
2.12. Dirección web de la Autoridad Reguladora del país miembro de la OCDE o de la autoridad reguladora del país adherente
del sistema de aceptación mutua de datos de esa organización, donde está
registrado o aprobado el IAGT que es objeto de solicitud (el registrante debe indicar la dirección exacta donde la Administración puede realizar esta
consulta).
|
|
3. Síntesis
del IAGT
|
|
( ) Local ( ) Importado 3.1 País de origen de la fábrica
de IAGT:
|
|
3.2 Nombre, dirección y origen
de la planta de fabricación del IAGT incluyendo calle, distrito o área,
estado, ciudad,
país:
|
|
3.3 Número de código
experimental que fue asignado por el fabricante en el caso de que exista
(el número de código experimental es la denominación utilizada por el fabricante para identificar el ingrediente activo del plaguicida
durante las primeras fases del desarrollo):
|
|
3.4 Empaque
o envase
|
|
3.5 Material:
|
3.6 Tipo:
|
3.7 Tamaño:
|
|
4.Lugar o medio donde recibir notificaciones (Dirección
Electrónica):
|
|
5.Observaciones:
|
|
Firma del representante legal:
|
Ficha articulo
ANEXO II
DECLARACIÓN JURADA
Para efectos de facilitar la presentación de la información que debe ser
presentada bajo fe de juramento, según lo dispuesto en el presente reglamento,
mediante declaración jurada notarial, el registrante podrá aportar en una sola
declaración jurada la información que se indica a continuación, ya sea persona
jurídica o persona física, utilizando como guía las plantillas siguientes:
DECLARACIÓN JURADA DE PERSONA JURÍDICA
NÚMERO XXX. Ante mí, XXX,
Notario Público con oficina en la ciudad de XXX, comparece el señor XXX, mayor,
XXX (estado civil), XXX (profesión u oficio), portador de la cédula de
identidad número XXX (o del pasaporte de su país número XXX), vecino de XXX, en
su condición de apoderado generalísimo sin límite de suma (o apoderado especial
para este acto) de la compañía XXX, cédula jurídica número XXX, personería de
la cual el suscrito Notario da fe con vista en el Registro de Personas
Jurídicas del Registro Público, bajo la cédula jurídica número ___________ (o
al tomo XXX, folio XXX, asiento XXX), quien bajo la fe del juramento declara lo
siguiente: PRIMERO.- Que mi representada está tramitando la solicitud de
registro de IAGT data completa por reconocimiento de evaluación de estudios
denominado: ___________________, concentración mínima de ____________ % (m/v o
m/m), fabricante ______________ (indicar nombre), dirección ________________,
país de origen _____________, cuyo material de envase es_____, con número o
código de registro o autorización ___________,en el país____________________
(miembro de la OCDE), a través de______________________ Autoridad Reguladora
del país OCDE o de la autoridad reguladora del país adherente del sistema de
aceptación mutua de datos de esa organización.-SEGUNDO.- Que los
estudios técnicos aportados como parte del trámite de solicitud de registro por
reconocimientos de evaluación de estudios corresponden a los mismos estudios
que fueron aprobados por la Autoridad Reguladora del país miembro de OCDE o de
la autoridad reguladora del país adherente del sistema de aceptación mutua de
datos de esa organización.TERCERO. Que el IAGT está aprobado en el país
OCDE o por el país adherente del sistema de aceptación mutua de datos de esa
organización que realizó las evaluaciones del plaguicida que se quiere
registrar en Costa Rica mediante este mecanismo y que dicho registro o autorización
se encuentra vigente, según registro o referencia de aprobación para su
verificación _________. CUARTO. - Que toda la información, estudios
técnicos y documentos del apartado I.A del Anexo III del Reglamento para
optar por el Registro de Ingrediente Activo Grado Técnico mediante el
reconocimiento de la evaluación de los estudios técnicos aprobados por las
Autoridades Reguladoras de los países miembros de la Organización para la Cooperación
y el Desarrollo Económicos (OCDE) o los países adherentes al Sistema de Aceptación
Mutua de Datos de la OCDE que se aportan para esta solicitud fueron
aprobados por la Autoridad Reguladora del país miembro de la OCDE o del país
adherente al sistema de aceptación mutua de datos de esa organización y que
sustentaron, dieron origen al registro o aprobación de este IAGT y que su
representada cuenta con la autorización del titular de registro ante el país
miembro de OCDE o país adherente indicado para someter esta información a la solicitud
de registro. QUINTA. Que existe una solicitud de registro de IAGT bajo
la modalidad de data completa pendiente de resolución ante el Servicio
Fitosanitario del Estado, para la misma entidad química, bajo el trámite N°
___________________ (en caso de ser procedente deberá así indicarlo). SEXTO.
Que exonero de toda responsabilidad a las autoridades del Ministerio de
Salud, Ministerio de Ambiente y Energía y el Servicio Fitosanitario del Estado-
Ministerio de Agricultura y Ganadería, con base en la información que es objeto
de la presente declaración. SÉTIMO. Que conozco que si las autoridades
competentes corroboran alguna
falsedad en la
presente declaración, errores, omisiones o incongruencias en los documentos aportados,
podrá aplicar las medidas y sanciones establecidas en la Ley General de Salud,
Ley de Protección Fitosanitaria y el resto del ordenamiento jurídico
costarricense, como lo son la cancelación del registro y el retiro del producto
del mercado entre otras. El suscrito Notario hace constar que advirtió al
compareciente sobre la trascendencia legal de sus manifestaciones, y de las
penas con que el Código Penal castiga los delitos de falso testimonio y de
perjurio. Es todo. Expido un primer testimonio. Leído lo anterior al
compareciente, manifiesta que lo aprueba y firmamos en la ciudad de XXX al ser
las XXX horas, del día XXX del año dos mil XXX----------------------------------------------------------------------trascripción
de firmas----------- --------------------------------------Lo anterior es copia
fiel y exacta de la escritura número XXX, visible al folio XXX, del tomo XXX,
del protocolo del suscrito Notario. Confrontado con su original resultó
conforme, y lo expido como un primer testimonio en el mismo acto y lugar de firmarse
la matriz.
Nota: Debe estamparse el
sello blanco del Notario, así como cancelar ¢275 en timbres del Colegio de
Abogados y ¢125 en timbres fiscales.
DECLARACIÓN JURADA DE PERSONA FÍSICA
NÚMERO XXX. Ante mí, XXX,
Notario Público con oficina en la ciudad de XXX, comparece el señor XXX, mayor,
XXX (estado civil), XXX (profesión u oficio), portador de la cédula de
identidad número XXX (o del pasaporte de su país número XXX), vecino de XXX, quien
bajo la fe del juramento declara lo siguiente: PRIMERO.- Que estoy
tramitando la solicitud de registro de IAGT data completa por reconocimiento de
evaluación de estudios denominado: ___________________, concentración mínima de
____________ % (m/v o m/m), fabricante ______________ (indicar nombre),
dirección ________________, país de origen _____________, cuyo material de
envase es_____, con número o código de registro o autorización ___________,en
el país____________________ (miembro de la OCDE), a través de______________________
Autoridad Reguladora del país OCDE o de la autoridad reguladora del país
adherente del sistema de aceptación mutua de datos de esa organización.- SEGUNDO.-
Que los estudios técnicos aportados como parte del trámite de solicitud de registro
por reconocimiento de evaluación de estudios corresponden a los mismos estudios
que fueron aprobados por la Autoridad Reguladora del país miembro de OCDE o de
la autoridad reguladora del país adherente del sistema de aceptación mutua de
datos de esa organización. TERCERO. Que el IAGT está aprobado en el país
OCDE o por el país adherente del sistema de aceptación mutua de datos de esa
organización que realizó las evaluaciones del plaguicida que se quiere
registrar en Costa Rica mediante este mecanismo y que dicho registro o autorización
se encuentra vigente, según registro o referencia de aprobación para su
verificación _________. CUARTO. - Que toda la información, estudios
técnicos y documentos del apartado I.A del Anexo III del Reglamento para
optar por el Registro de Ingrediente Activo Grado Técnico mediante el
reconocimiento de la evaluación de los estudios técnicos aprobados por las
Autoridades Reguladoras de los países miembros de la Organización para la Cooperación
y el Desarrollo Económicos (OCDE) o los países adherentes al Sistema de Aceptación
Mutua de Datos de la OCDE que se aportan para esta solicitud fueron
aprobados por la Autoridad Reguladora del país miembro de la OCDE o del país
adherente al sistema de aceptación mutua de datos de esa organización y que
sustentaron, dieron origen al registro o aprobación de este IAGT y que quien
suscribe cuenta con la autorización del titular de registro ante el país
miembro de OCDE o país adherente indicado para someter esta información a la solicitud
de registro. QUINTA. Que existe una solicitud de registro de IAGT bajo
la modalidad de data completa pendiente de resolución ante el Servicio
Fitosanitario del Estado, para la misma entidad química, bajo el trámite N°
___________________ (en caso de ser procedente deberá así indicarlo). SEXTO.
Que exonero de toda responsabilidad a las autoridades del Ministerio de
Salud, Ministerio de Ambiente y Energía y el Servicio Fitosanitario del Estado-
Ministerio de Agricultura y Ganadería, con base en la información que es objeto
de la presente declaración. SÉTIMO. Que conozco que, si las autoridades
competentes corroboran alguna falsedad en la presente declaración, errores,
omisiones o incongruencias en los documentos aportados, podrá aplicar las
medidas y sanciones establecidas en la Ley General de Salud, Ley de Protección
Fitosanitaria y el resto del ordenamiento jurídico costarricense, como lo son
la cancelación del registro y el retiro del producto del mercado entre otras.
El suscrito Notario hace constar que advirtió al compareciente sobre la
trascendencia legal de sus manifestaciones, y de las penas con que el Código
Penal castiga los delitos de falso testimonio y de perjurio. Es todo. Expido un
primer testimonio. Leído lo anterior al compareciente, manifiesta que lo aprueba
y firmamos en la ciudad de XXX al ser las XXX horas, del día XXX del año dos
mil XXX----------------------------------------------------------------------trascripción
de firmas----------- --------------------------------------Lo anterior es copia
fiel y exacta de la escritura número XXX, visible al folio XXX, del tomo XXX,
del protocolo del suscrito Notario. Confrontado con su original resultó
conforme, y lo expido como un primer testimonio en el mismo acto y lugar de firmarse
la matriz.
Nota: Debe estamparse el
sello blanco del Notario, así como cancelar ¢275 en timbres del Colegio de
Abogados y ¢125 en timbres fiscales.
Ficha articulo
ANEXO III
REQUISITOS PARA EL REGISTRO DE INGREDIENTE ACTIVO GRADO TÉCNICO
MEDIANTE EL RECONOCIMIENTO DE LA EVALUACIÓN APROBADA DE LOS
ESTUDIOS TÉCNICOS POR PARTE DE LAS AUTORIDADES REGULADORAS DE
LOS PAÍSES MIEMBROS DE LA OCDE O DE LAS AUTORIDADES REGULADORAS
DE LOS PAÍSES ADHERENTES DEL SISTEMA DE ACEPTACIÓN MUTUA DE
DATOS DE LA OCDE
I. REQUISITOS DEL LEGAJO TÉCNICO PARA RECONOCIMIENTO DE
LA EVALUACIÓN DE LOS ESTUDIOS POR LA AUTORIDAD
REGULADORA DE LOS PAÍSES MIEMBROS DE OCDE O DE LAS
AUTORIDADES REGULADORAS DE LOS PAÍSES ADHERENTES DEL
SISTEMA DE ACEPTACIÓN MUTUA DE DATOS DE LA OCDE.
A. LEGAJO TÉCNICO
1) Estudios para la determinación de las propiedades físicas y químicas,
así como su
respectivo refrendo
químico. El fabricante del IAGT o de la sustancia purificada
utilizada para la
realización del estudio debe coincidir con el que se quiere registrar.
1.1 Estado físico.
1.2 Color.
1.3 Olor.
1.4 Punto de fusión en °C (sólidos).
1.5 Punto de ebullición en °C (líquidos) o punto de descomposición.
1.6 Densidad aparente para sólidos y densidad relativa para líquidos.
1.7 Presión de vapor, para sustancias con punto de ebullición mayor o
igual a 30°C.
1.8 Solubilidad en agua.
1.9 Solubilidad en solventes orgánicos en un solvente polar a elección y
también un solvente no polar a elección.
1.10 Punto de ignición.
1.11 Inflamabilidad (sólidos).
1.12 Punto de inflamación (líquidos).
1.13 Tensión superficial.
1.14 Propiedades explosivas.
1.15 Propiedades oxidantes.
1.16 Constante de disociación en agua.
2) Métodos analíticos y validación:
2.1 Método analítico y su respectiva validación para la determinación de
la concentración del ingrediente activo grado técnico.
2.2 Método analítico y su respectiva validación para la determinación en
el aire del ingrediente activo. Estos serán requeridos para productos
volátiles.
2.3 Método analítico y su respectiva validación para determinar los
residuos del ingrediente activo en los cultivos o en las cosechas donde se
aplique el producto.
2.4 Método analítico y su respectiva validación para determinar los
residuos del ingrediente activo en agua.
2.5 Método analítico y su respectiva validación para determinar los
residuos del ingrediente activo en suelo.
2.6 Método analítico y su respectiva validación para la determinación de
productos de degradación, impurezas relevantes que puedan haberse formado,
según consideraciones técnicas, durante el proceso de fabricación o
degradación.
3) Impacto en la salud humana y animal
Se deben presentar los siguientes estudios, que incluyan la portada,
introducción, materiales, métodos, resultados, referencias y las tablas de
datos consolidados que respalden los resultados. Los anexos con el registro de
los datos diarios, fotos, figuras, protocolos, cromatogramas, hojas
estadísticas no son necesarios para el análisis. Dicho análisis se llevará a
cabo solo en caso de duda razonable sobre los datos indicados en el reporte de
evaluación emitido por la Autoridad Reguladora.
a. Absorción, distribución, excreción y metabolismo en mamíferos
(Absorption,
distribution, excretion and metabolism in mammals).
i. Tasa y extensión de la absorción (Rate and extent of absorption).
ii. Distribución (Distribution).
iii. Potencial de acumulación (Potential or accumulation).
iv. Tasa y extensión de la excreción (Rate and extent of excretion).
v. Metabolismo en animales (Metabolism in animals).
vi. Compuestos de significancia toxicológica (Toxicologically
significant compounds: animals, plants and environment).
b. Toxicidad aguda (Acute toxicity)
i. DL50 oral en rata (Rat LD50 oral).
ii. DL50 dermal en rata (Rat LD50 dermal).
iii. CL50 inhalatoria en rata (Rat LC50 inhalation).
iv. Irritación dermal (Skin irritation).
v. Irritación ocular (Eye irritation).
vi. Sensibilidad dermal (Skin sensitization: test method used and
result).
c. Toxicidad a corto plazo (Short term toxicity)
i. Objetivo / Efecto crítico (Target / critical effect).
ii. NOAEL / NOEL relevante más bajo oral (Lowest relevant oral NOAEL / NOEL).
iii. NOAEL / NOEL relevante más bajo dermal (Lowest relevant dermal
NOAEL / NOEL).
iv. NOAEL / NOEL relevante más bajo inhalatorio (Lowest relevant inhalation
NOAEL / NOEL).
d. Genotoxicidad (Genotoxicity)
e. Toxicidad a largo plazo y carcinogenicidad (Long term toxicity and
carcinogenicity)
i. Objetivo / Efecto crítico (Target/critical effect).
ii. NOAEL / NOEL relevante más bajo (Lowest relevant NOAEL / NOEL).
iii. Carcinogenicidad (Carcinogenicity).
f. Toxicidad reproductiva (Reproductive toxicity)
i. Objetivo para la reproducción / Efecto crítico (Reproduction target /
critical effect).
ii. NOAEL / NOEL relevante más bajo reproductivo (Lowest relevant reproductive
NOAEL / NOEL).
iii. Objetivo para el desarrollo (Developmental target / critical
effect).
iv. NOAEL / NOEL relevante más bajo para el desarrollo (Lowest relevant developmental
NOAEL / NOEL).
g. Neurotoxicidad / Neurotoxicidad tardía (Neurotoxicity / Delayed
neurotoxicity)
i. Neurotoxicidad aguda (Acute neurotoxicity).
ii. Neurotoxicidad subcrónica (Subchronic neurotoxicity).
h. Otros estudios toxicológicos (Other toxicological studies). Para este
apartado deben proporcionarse en caso de que la Autoridad Reguladora del país
OCDE haya solicitado información adicional para autorizar el registro del IAGT.
i. Datos médicos (Medical data).
j. Absorción dermal (Dermal absorption).
4) Residuos
a) LMR propuestos (Proposed MRL's). Para este apartado deben presentarse
sólo los resultados puntuales obtenidos en los estudios.
5) Estudios ecotoxicológicos:
Se deben presentar los siguientes estudios, que incluyan la portada,
introducción, materiales, métodos, resultados, referencias y las tablas de
datos consolidados que respalden los resultados.
Los anexos con el registro de los datos diarios, fotos, figuras,
protocolos, cromatogramas, hojas estadísticas no son necesarios para el
análisis. Dicho análisis se llevará a cabo solo en caso de duda razonable sobre
los datos indicados en el reporte de evaluación emitido por la Autoridad Reguladora.
Con respecto a las guías indicadas en este apartado son las recomendadas
y se citan para claridad del registrante sobre el tipo de estudio requerido.
Sin embargo, los estudios pueden haberse realizado con guías diferentes siempre
y cuando correspondan con los estudios aprobados por las autoridades
reguladoras en el país miembro de la OCDE o las autoridades reguladoras en el
país adherente del sistema de aceptación mutua de datos de la OCDE y cuyos datos
constan en el reporte de evaluación emitido por la Autoridad Reguladora de
dicho país.
5.1.Estudio de toxicidad oral aguda en aves. Debe cumplir lo indicado en
la guía OCSPP 850.21, o cualquier otra internacionalmente reconocida.
5.2.Estudio de efectos sobre la reproducción en aves. Debe cumplir lo
indicado en las guías OECD 206 y OCSPP 850.2300, o cualquier otra
internacionalmente reconocida.
5.3.Estudio de toxicidad oral aguda para las abejas. Debe cumplir lo
indicado en la guía OECD 213, o cualquier otra internacionalmente reconocida.
5.4.Estudio de toxicidad por contacto aguda para las abejas. Debe
cumplir lo indicado en las guías OECD 214 y OCSPP 850.3020, o cualquier otra internacionalmente
reconocida.
5.5.Estudio de toxicidad para lombriz de tierra. Debe cumplir lo
indicado en las guías OCSPP 850.3100, OECD 222 u OECD 207, o cualquier otra internacionalmente
reconocida.
5.6.Estudio de toxicidad para la comunidad de microorganismos del suelo:
transformación de nitrógeno. Debe cumplir lo indicado en las guías OECD 216 y
OCSPP 850.5100, o cualquier otra internacionalmente reconocida.
5.7.Estudio de toxicidad para la comunidad de microorganismos del suelo:
respiración. Debe cumplir lo indicado en las guías OECD 217 y OCSPP 850.5100, o
cualquier otra internacionalmente reconocida.
5.8.Estudio de toxicidad aguda en peces. Debe cumplir lo indicado en las
guías OECD 203 y OCSPP 850.1075, o cualquier otra internacionalmente reconocida.
5.9. Estudio de toxicidad prolongada para peces. Es preferible que sea
un estudio realizado con la(s) misma(s) especie(s) presentada(s) en el estudio
de toxicidad aguda. Debe presentar alguno de dos tipos de estudios según
corresponda con las propiedades del IAGT que se señalan:
5.9.1. Para todos los casos se debe presentar un estudio de toxicidad en
las primeras fases de la vida de los peces. Debe cumplir lo indicado en las guías
OECD 210 y OCSPP 850.1400, o cualquier otra internacionalmente reconocida.
5.9.2. Se debe presentar un estudio sobre el ciclo vital de los peces
que debe cumplir lo indicado en las guías OCSPP 850.1500 cuando se cumpla alguna
de las siguientes condiciones:
5.9.2.1. El factor de bioacumulación sea superior a 1000
5.9.2.2. La sustancia sea persistente en agua o en sedimento (DT50 >
60 días)
5.9.2.3. Del estudio de toxicidad aguda en peces se desprendan valores
de EC50 inferiores a 0.1 mg/L.
5.10. Estudio de bioacumulación en peces. Debe cumplir lo indicado en
las guías OECD 305 y OCSPP 850.1730, o cualquier otra internacionalmente reconocida.
Solo debe presentarse si se cumple alguno de los siguientes criterios:
5.10.1. Cuando el coeficiente N- octanol/agua (LogPOW) sea mayor o igual
a 3.
5.10.2. El producto es persistente en el agua (DT50 >60 días).
5.11. Estudio de toxicidad aguda en Daphnia magna. Debe cumplir lo
indicado en las guías OECD 202 y OCSPP 850.1010, o cualquier otra
internacionalmente reconocida
5.12.Estudio de toxicidad crónica en Daphnia magna. Debe cumplir lo
indicado en las guías OECD 211 y OCSPP 850.1300, o cualquier otra
internacionalmente reconocida.
5.13.Estudio de toxicidad en algas. Debe cumplir lo indicado en las
guías OECD 201 y OCSPP 850. 5400, o cualquier otra internacionalmente
reconocida.
6. Estudios de destino ambiental
Se deben presentar los siguientes estudios, que incluyan la portada,
introducción, materiales, métodos, resultados, referencias y las tablas de
datos consolidados que respalden los resultados.
Los anexos con el registro de los datos diarios, fotos, figuras,
protocolos, cromatogramas, hojas estadísticas no son necesarios para el
análisis. Dicho análisis se llevará a cabo solo en caso de duda razonable sobre
los datos indicados en el reporte de evaluación emitido por la Autoridad Reguladora.
Con respecto a las guías indicadas en este apartado son las recomendadas
y se citan para claridad del registrante sobre el tipo de estudio requerido.
Sin embargo, los estudios pueden haberse realizado con guías diferentes siempre
y cuando correspondan con los estudios aprobados por las autoridades
reguladoras en el país miembro de la OCDE o las autoridades reguladoras en el
país adherente del sistema de aceptación mutua de datos de la OCDE y cuyos datos
constan en el reporte de evaluación emitido por la Autoridad Reguladora de
dicho país.
6.1.Estudio sobre degradación aeróbica en el suelo. Debe cumplir lo
indicado en las guías OECD 307 y OCSPP 835.4100, o cualquier otra
internacionalmente reconocida.
6.2.Estudio sobre adsorción y desorción. Debe cumplir lo indicado en las
guías OECD 106 y OCSPP 835. 1230, o cualquier otra internacionalmente reconocida.
6.3.Estudio sobre lixiviación en suelo. Debe cumplir lo indicado en las
guías OECD 312 y OCSPP 835. 1240. Solo se requiere si de los datos obtenidos
del estudio de adsorción y desorción se determina un valor de Koc < 15 ml/g,
o cualquier otra internacionalmente reconocida.
6.4.Estudio sobre degradación aeróbica en agua. Debe cumplir lo indicado
en las guías OECD 308 y OCSPP 835.4400 u OCSPP 835 4300, o cualquier otra internacionalmente
reconocida.
6.5.Estudio sobre hidrólisis. Debe cumplir lo indicado en las guías OECD
111 y OCSPP 835.2120 u 835.2130, o cualquier otra internacionalmente
reconocida.
6.6.Estudio sobre fotólisis acuosa. Debe cumplir lo indicado en las
guías OECD 316 y OCSPP 835.2210 u 835.2240, o cualquier otra internacionalmente
reconocida.
6.7.Estudio del coeficiente de partición n-octanol / agua (KO/W). Debe
cumplir lo indicado en la guía OECD 122, o cualquier otra internacionalmente
reconocida.
II. REQUISITOS QUE SERÁN EVALUADOS EN EL ANÁLISIS DE FONDO
PARA REGISTRO DE IAGT
A. LEGAJO ADMINISTRATIVO
1. Solicitud de registro (Anexo I del presente reglamento).
2. Comprobante de pago del arancel vigente.
3. Hoja de seguridad del ingrediente activo grado técnico, debe contener
los requisitos estandarizados internacionalmente utilizando como modelo los
lineamientos del Sistema Globlamente Armonizado de clasificación y etiquetado
de productos químicos (GHS, por sus siglas en inglés) de las Naciones Unidas".
4. Etiqueta de acuerdo con lo dispuesto en el Reglamento Técnico
Centroamericano de etiquetado vigente. La información presente en la etiqueta
debe concordar con lo indicado en el expediente.
5. Fórmula estructural del IAGT que se quiere registrar (debe incluir la
estereoquímica de isómeros activos si se conocen).
Nota 1: En caso de no ser
los titulares de registro en el país de referencia, debe presentar una carta
del titular del registro del IAGT de origen al que se solicita el
reconocimiento, autorizando expresamente a la empresa que desea registrar para
que pueda utilizar la información y pueda realizar el reconocimiento a nombre
de la empresa registrante. En caso que la declaración jurada y las
autorizaciones indicadas en este ordinal fuesen otorgadas en el extranjero,
debe cumplir con el proceso de legalización o apostilla de documentos.
Nota 2: En caso de que la
solicitud de registro sea firmada por el representante de una persona jurídica,
deberá demostrar tener poder suficiente para hacerlo, mediante certificación
que acredite la personería y el carácter con el que actúa el firmante
Nota 3: La solicitud de
registro y toda la información presentada tendrá carácter de declaración jurada.
B. LEGAJO CONFIDENCIAL
La información confidencial debe ser presentada por duplicado en un sobre,
cuyos folios, original y copia, serán sellados por el funcionario receptor,
siendo devuelta la copia al registrante. En caso de presentar la información de
forma física, la autoridad procederá a cerrar y lacrar el sobre, mismo que
ambos firmarán de forma tal que cuando el sobre sea abierto por el funcionario
responsable de la información confidencial tenga la certeza que la confidencialidad
no ha sido violada, en caso de no seguirse el anterior procedimiento y formalidades,
la AC no recibirá la información. Dentro del sobre el registrante deberá
presentar la siguiente información:
1. Certificado de composición cualitativa cuantitativa del ingrediente
activo grado técnico emitido por la casa matriz o por el fabricante con su
respectivo refrendo químico. Se debe indicar la identidad del ingrediente
activo, impurezas y aditivos (éste último cuando corresponda y aplique al caso
concreto) de acuerdo a su nombre químico según IUPAC y el número CAS cuando
estén disponibles, en caso de no estar disponible, se debe presentar la
estructura química. Los resultados obtenidos en el estudio de cinco lotes deben
cumplir con los límites establecidos en el certificado de composición. Se deberá
presentar firmado en original, copia confrontada o copia autenticada por un notario
público, el cual contendrá:
1.1 Concentración mínima del ingrediente activo en el IAGT expresado en
porcentaje m/m (o g/kg) o porcentaje m/v. En el caso de indicarse la
concentración en m/v debe declararse la densidad.
1.2 Concentración máxima de cada impureza mayor o igual a un gramo por
kilogramo (1 g/kg) ó 0,1%m/m.
1.3 Concentración máxima de impurezas relevantes, en el caso de no estar
presentes se deberá indicar la no presencia de las mismas.
1.4 Concentración mínima y máxima de otros aditivos presentes,
expresados en g/kg ó porcentaje, cuando corresponda y aplique al caso concreto.
Debe indicar la función (por ejemplo, estabilizante).
1.5 En caso de que el ingrediente activo sea un TK, deberá también
presentarse la concentración en base seca y deberá indicarse el límite máximo y
mínimo en la especificación.
2. Estudio de cinco lotes con la totalidad de las páginas indicadas en
la portada, realizado con el IAGT que se quiere registrar (debe coincidir el
fabricante y origen). Típicamente la fracción no identificada y no
contabilizada del ingrediente activo grado técnico TC/TK no debe exceder de
veinte gramos por kilogramo. Se deben anexar los análisis y cromatogramas (con
su área respectiva) correspondientes a cada lote muestreado e incluir los datos
necesarios para la reproducción de los resultados obtenidos o una muestra de
cálculo en donde quede claro cómo se obtuvo el resultado tanto para el IAGT como
para las impurezas.
3. Justificación de la determinación de los límites de fabricación
establecidos para el ingrediente activo grado técnico e impurezas. Se deben
explicar las bases estadísticas u otros criterios técnicos utilizados para
establecer los límites de fabricación y se deberá aportar la justificación
técnica respectiva de cómo se llegaron a obtener los mismos para ser evaluados
por la AC. En caso de que no sea un criterio estadístico, se deberá aportarse
datos de apoyo para dar mayor justificación a la especificación técnica. Los criterios
de experto no se consideran válidos sin una base científica que los respalde.
4. Análisis de la identidad del ingrediente activo purificado
sintetizado por el fabricante que consta en la solicitud: el cual estará
constituido por un conjunto de determinaciones analíticas que permitan
establecer la composición y la constitución del ingrediente activo en forma
inequívoca. Para ello se deberán presentar dos espectros del ingrediente activo
con su debida interpretación, de entre los siguientes: IR, RMN, Masas y UV-VIS,
debiendo presentar al menos uno entre RMN o Masas o ambos. En caso de duda la
AC, mediante resolución razonada, podrá solicitar una prueba adicional.
5. Identidad de las impurezas o eventualmente grupos de impurezas
relacionadas presentes en el ingrediente activo sintetizado por el fabricante
que consta en el certificado de composición, deberán ser identificadas mediante
análisis químicos y espectroscópicos con su debida interpretación que permitan
concluir indubitable e inequívocamente a la identidad de cada impureza o grupo
de impurezas relacionadas.
6. Justificación de la presencia de impurezas: el registrante debe
proveer las explicaciones técnicas necesarias sobre la presencia de las
impurezas en el producto. La justificación debe basarse en fundamentos
químicos. Si la AC determina que una impureza relevante puede estar presente,
solicitará la justificación técnica del por qué no ha sido declarada.
7. Métodos Analíticos y su respectiva validación para determinar las
impurezas mayores o iguales a un gramo por kilogramo (1 g/kg) o 0,1% m/m. En
caso de no presentar el estudio completo por considerar innecesario algún anexo
(por ejemplo la foto del equipo utilizado en la determinación), se debe
justificar técnicamente por qué no se considera necesario la no presentación de
este.
8. Resumen de la vía de fabricación. Para cada proceso resultante en un
ingrediente activo grado técnico, debe proveerse la siguiente información:
8.1 Caracterización general del proceso.
8.2 Diagrama de flujo de fabricación.
8.3 Identificación de los materiales usados para producir el producto.
8.4 Descripción general de las condiciones que se controlan durante el
proceso, según sea el caso: temperatura, presión, pH y humedad.
Ficha articulo
ANEXO IV
FORMULARIO DE RECOPILACIÓN DE DATOS TÉCNICOS
DEL REPORTE DE
EVALUACIÓN
Cuadro l. Resumen de datos de identificación
del producto y propiedades físicas y
químicas del
Reporte de Evaluación
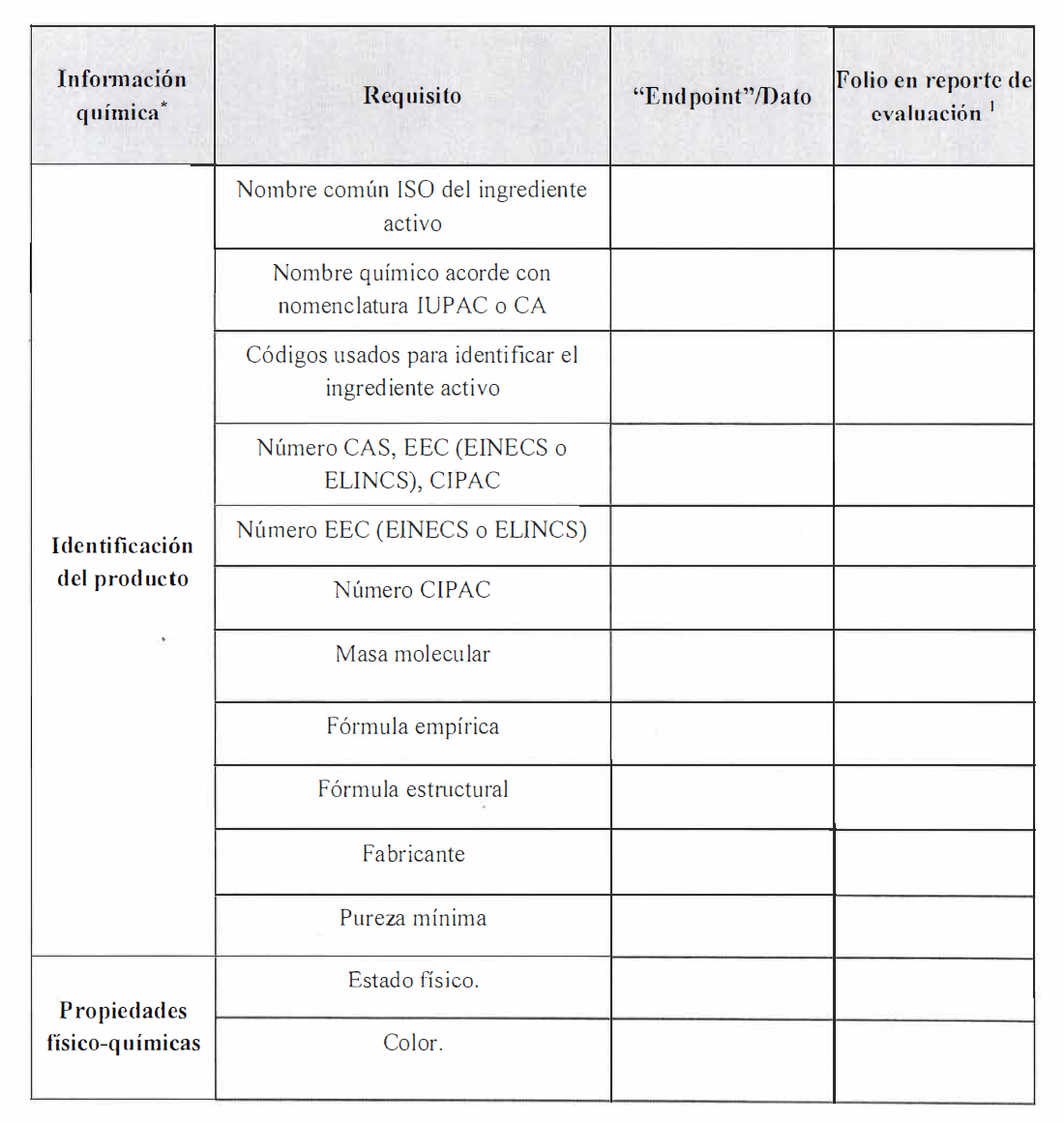
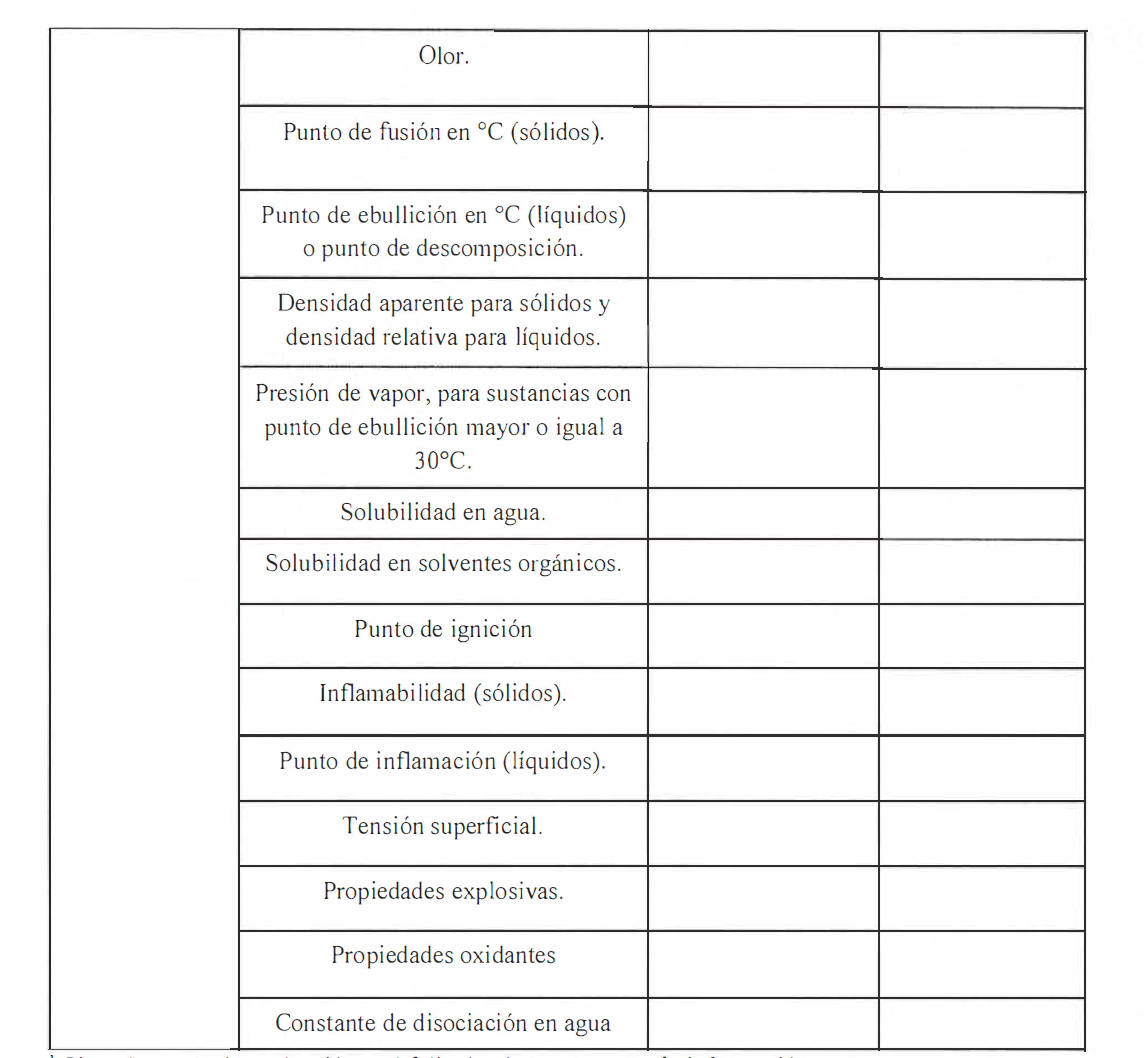
1 Citar el repo1ie de evaluación y el folio
donde se encuentra la información
* En esta tabla resumen de información química
no se incluyeron los requisitos de los métodos analíticos ni la información del
legajo confidencial ni administrativo.
Cuadro 2. Resumen de datos de impacto en la salud humana y animal
extraídos
del Reporte de Evaluación
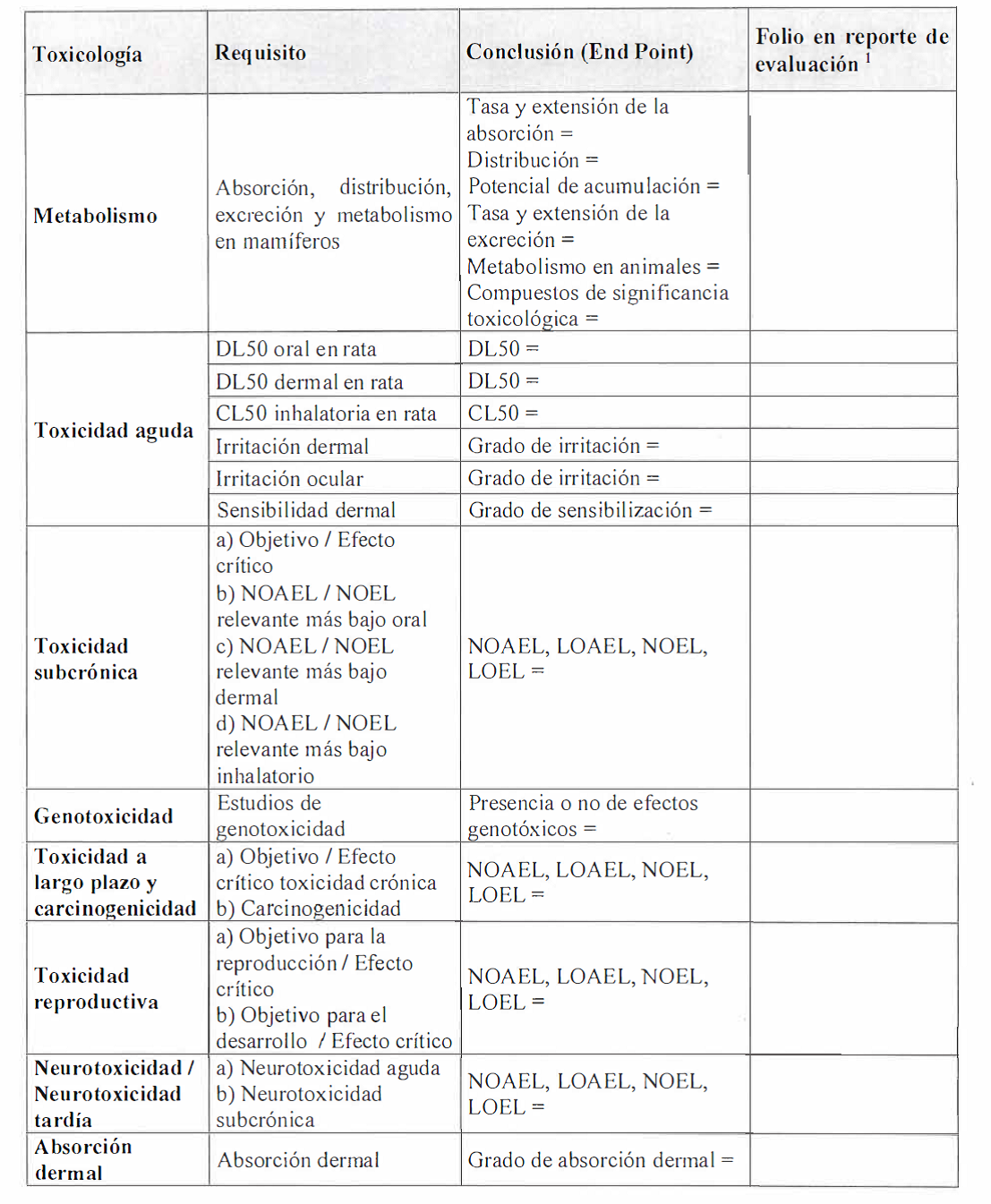
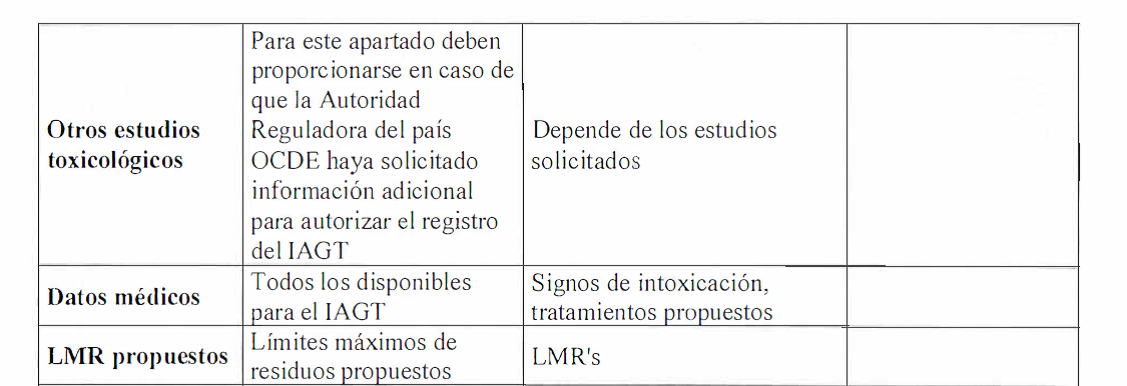
1 Citar el repmie de evaluación y el folio donde se
encuentra la información
Cuadro 3. Resumen de datos ecotoxicológicos
extraídos del Reporte de Evaluación.
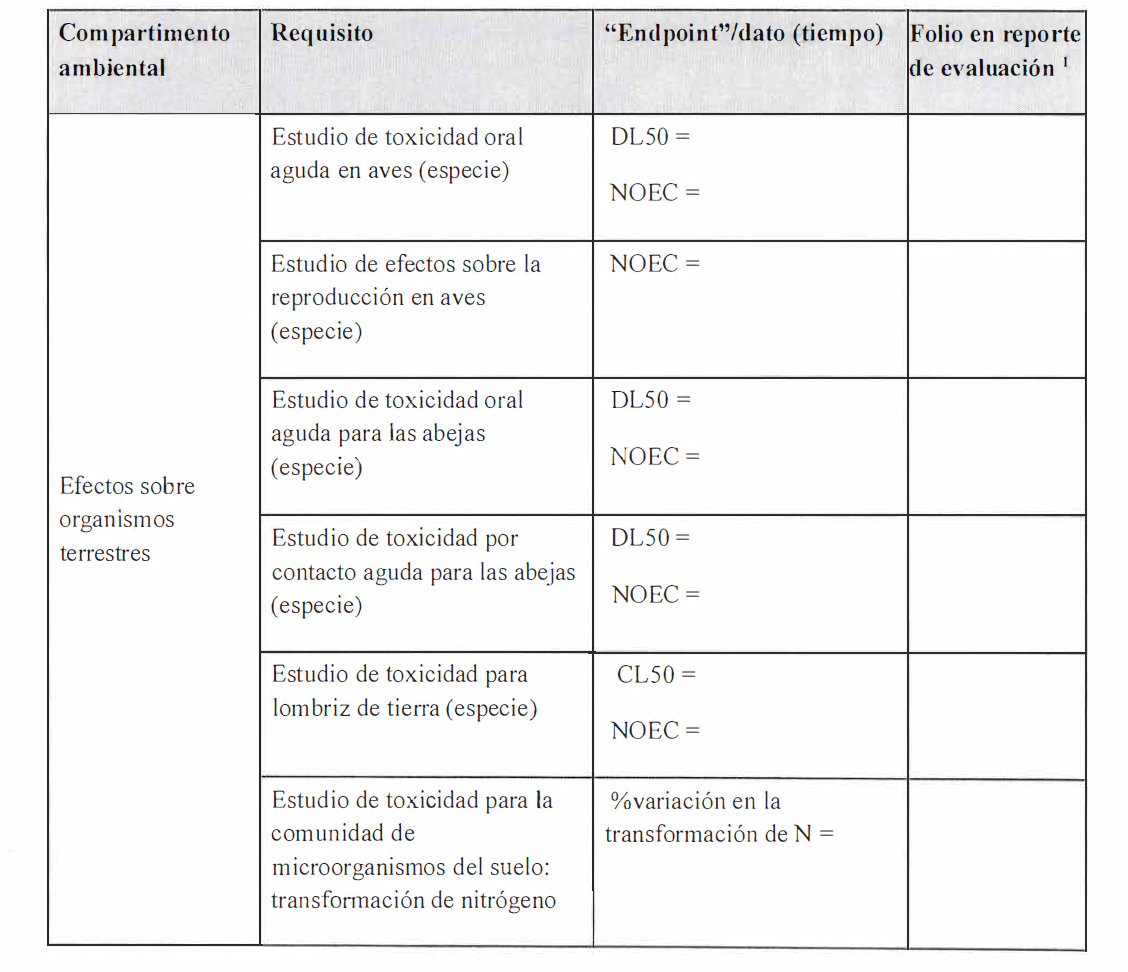
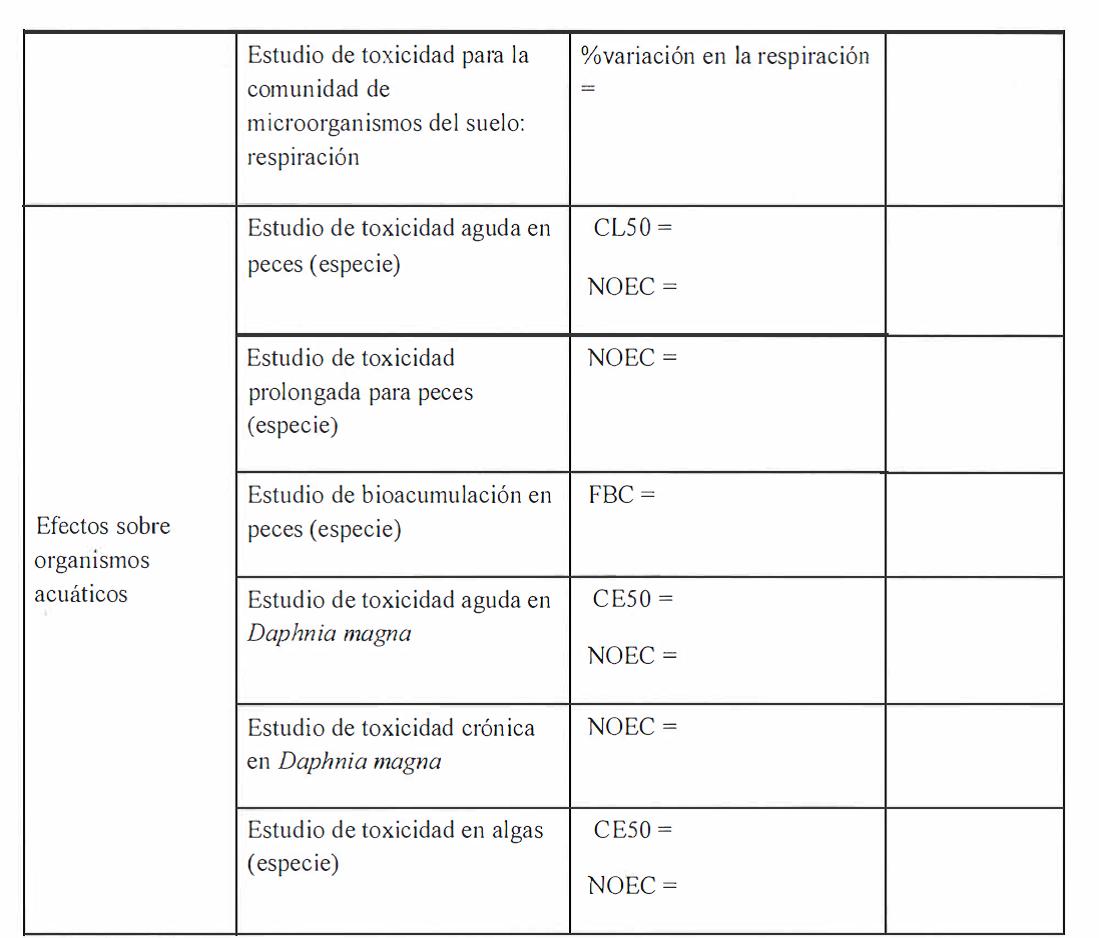
1 Citar el repo,te de evaluación y el folio donde se
encuentra la información
Cuadro 4. Resumen de datos de destino y
comportamiento ambiental extraídos del Reporte de Evaluación
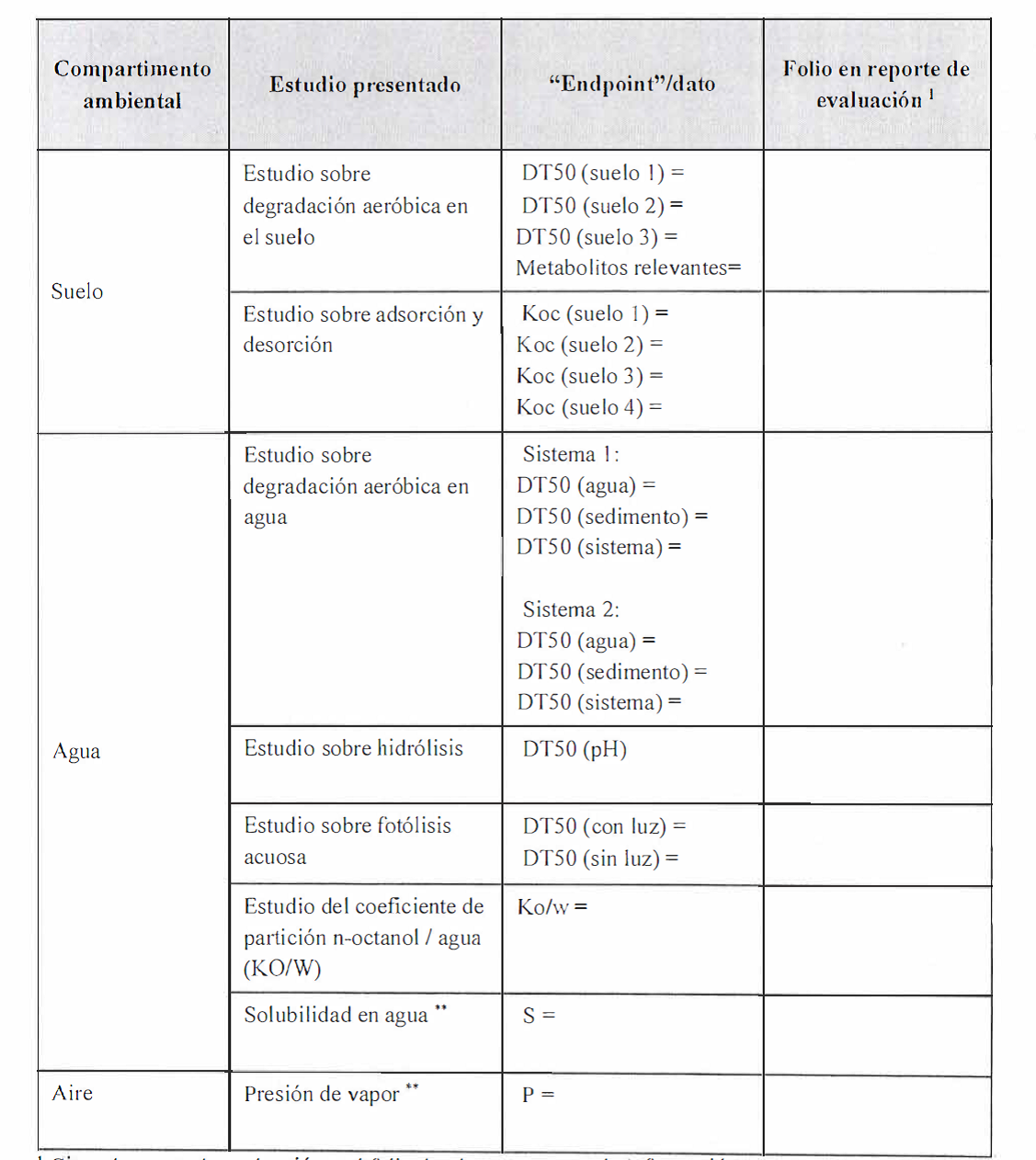
1 . , Citar el reporte de evaluac1on y el folio
donde se encuentra la mformación
** Estos datos se toman del informe químico de la
autoridad revisora competente, por cuanto son necesarios para la evaluación
ambiental."
(Así
reformado por el artículo 2° del decreto ejecutivo N° 43563 del 28 de mayo de
2022)
Ficha articulo
Fecha de generación: 15/1/2025 02:28:19
|